

1) Общая формула вещества - CxHyBrz
Вычислим количества вещества углекислого газа, воды и бромоводорода
n(CO2) = 4,48 : 22,4 = 0,2 моль; n(C) = n(CO2) = 0,2 моль
n(H2O) = 0,9 : 18 = 0,05 моль;
n(HBr) = 16,2 : 81 = 0,2 моль;
n(H) = 2n(H2O) + n(HBr) = 0,05 ⋅ 2 + 0,2 = 0,3 моль
n(Br) = n(HBr) = 0,2 моль
Соотношение: n(C) : n(H) : n(Br) = 0,2 : 0,3 : 0,2 = 2 : 3 : 2 = 4 : 6 : 4
x : y : z = 4 : 6 : 4
Молекулярная формула - C4H6Br4
2) Структурная формула вещества A:
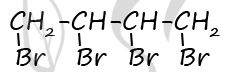

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7761.
1) Уравнения реакций
H2SO4 + BaO2 = BaSO4↓ + H2O2 (1)
2H2O2 = (кат. MnO2) 2H2O + O2↑ (2)
2) Вычислим количество воды в исходном растворе
Δm = m(O2) = 6,4 г
n(O2) = 6,4 : 32 = 0,2 моль
2n(O2) = n(H2O2) = n(H2SO4) = 0,4 моль (по уравнению 1 и 2)
m(H2SO4) = 0,4 ⋅ 98 = 39,2 г
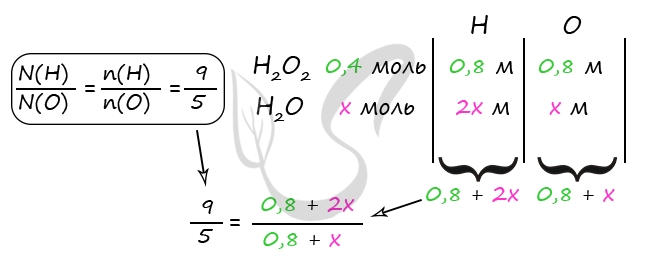
Примем n(H2O) = x моль
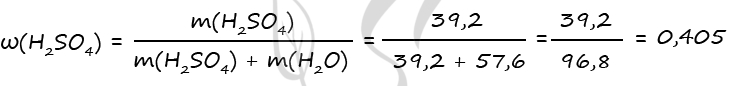
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7760.
Верный ответ: 446,7
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7753.
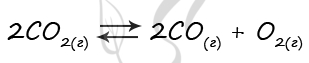
Верный ответ: 13
Таблица (по условиям)
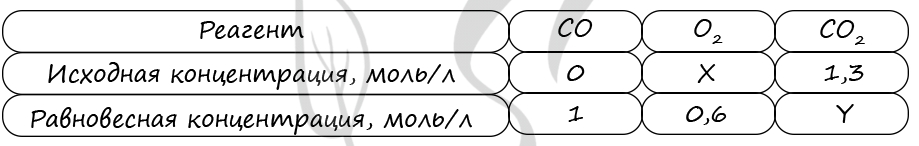
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7732.
1) Общая формула вещества - CxHyOz
Вычислим количество вещества продуктов
n(CO2) = 70,4 : 44 = 1,6 моль
n(C) = n(CO2) = 1,6 моль
n(H2O) = 36,0 : 18 = 2 моль
n(H) = 2n(H2O) = 2 ⋅ 2 = 4 моль
m(H) = 4 ⋅ 1 = 4 г
m(O) = 29,6 - 1,6 ⋅ 12 - 4 = 6,4 г
n(O) = 6,4 : 16 = 0,4 моль
Определена молекулярная масса вещества
M(CxHyOz)по услов. = 2,552 ⋅ 29 = 74 г/моль
x : y : z = 1,6 : 4 : 0,4 = 4 : 10 : 1
Вычисленная формула - C4H10O
M(CxHyOz)вычисл = 74 г/моль
Молекулярная формула исх. в-ва - C4H10O
2) Структурная формула вещества
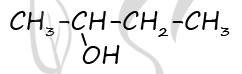
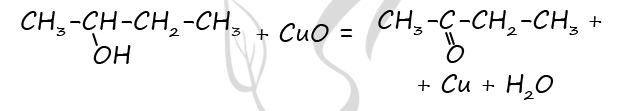
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7726.