

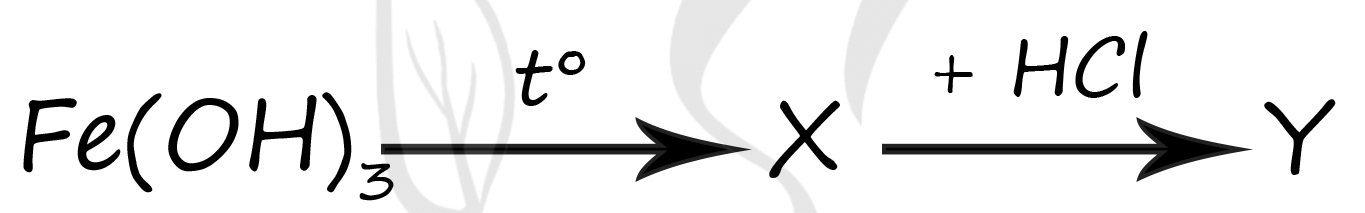
1) FeCl3
2) FeO
3) Fe2O3
4) FeCl2
5) Fe(OH)3
Верный ответ: 31
Вещество X - (3) - Fe2O3
Нерастворимые гидроксиды при термическом разложении легко отдают воду и образуют оксид металла в соответствующей степени окисления (+3)
2Fe(OH)3 = Fe2O3 + 3H2O
Вещество Y - (1) - FeCl3
Происходит обычная реакция обмена, в которой никто степени окисления не меняет, поэтому образуется именно хлорид железа (III)
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7526.
Верный ответ: 1243
В этом задании скрыты 60 реакций! Правильный подход к его выполнению может значительно повысить ваш уровень знаний неорганической химии.
Итак, ключевой момент: нужно попробовать составить реакцию каждого из веществ (А, Б, В, Г) со всеми предложенными реагентами! Вы должны узнать, возможна ли каждая из этих реакций, или понять причину, по которой она невозможна (например, в реакции не может быть два осадка: и справа, и слева). Следуйте такому подходу, и вы удивитесь, как быстро повысится ваш "неорганический уровень" ;)
Реакции для K2Cr2O7 протекают так:
K2Cr2O7 + 14HI = 2KI + 2CrI3 + 3I2 + 7H2O
K2Cr2O7 + 14HCl = 2KCl + 2CrCl3 + 7H2O + 3Cl2
K2Cr2O7 + 2KOH = 2K2CrO4 + H2O
Реакции для FeBr2 протекают так:
FeBr2 + 2NaOH = Fe(OH)2 + 2NaBr
2FeBr2 + 3Cl2 = 2FeCl3 + 2Br2
FeBr2 + 2AgNO3 = Fe(NO3)2 + 2AgBr
Реакции для SiO2 протекают так:
SiO2 + 2NaOH = Na2SiO3 + H2O
SiO2 + 4HF = SiF4 + 2H2O
SiO2 + 2C = Si + 2CO
Реакции для S протекают так:
S + H2 = H2S
3S + 6NaOH = 2Na2S + Na2SO3 + 3H2O
S + 6HNO3 = H2SO4 + 6NO2 + 2H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7524.
1) сульфат меди(II)
2) соляная кислота
3) сульфат железа(II)
4) гидроксид натрия
5) нитрат кальция
Верный ответ: 41
Вещество X - NaOH (4)
Вещество Y - CuSO4 (1)
В результате реакции между гидроксидом натрия и сульфатом меди (II) → образуется сульфат натрия и осадок голубого цвета - гидроксид меди (II)
CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7523.
1) 2C + O2 = (t°) 2CO
2) Fe2O3 + 3CO = (t°) 2Fe + 3CO2
3) 2Fe + 6H2SO4 = (t°) Fe2(SO4)3 + 3SO2↑ + 6H2O
4) Fe2(SO4)3 + Cu = 2FeSO4 + CuSO4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7513.
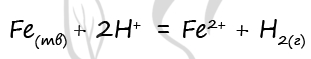
Верный ответ: 24
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7466.