


Для выполнения заданий 1-3 используйте следующий ряд химических элементов:
Ответом в заданиях 1-3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Верный ответ: 24
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6922.
Верный ответ: 152
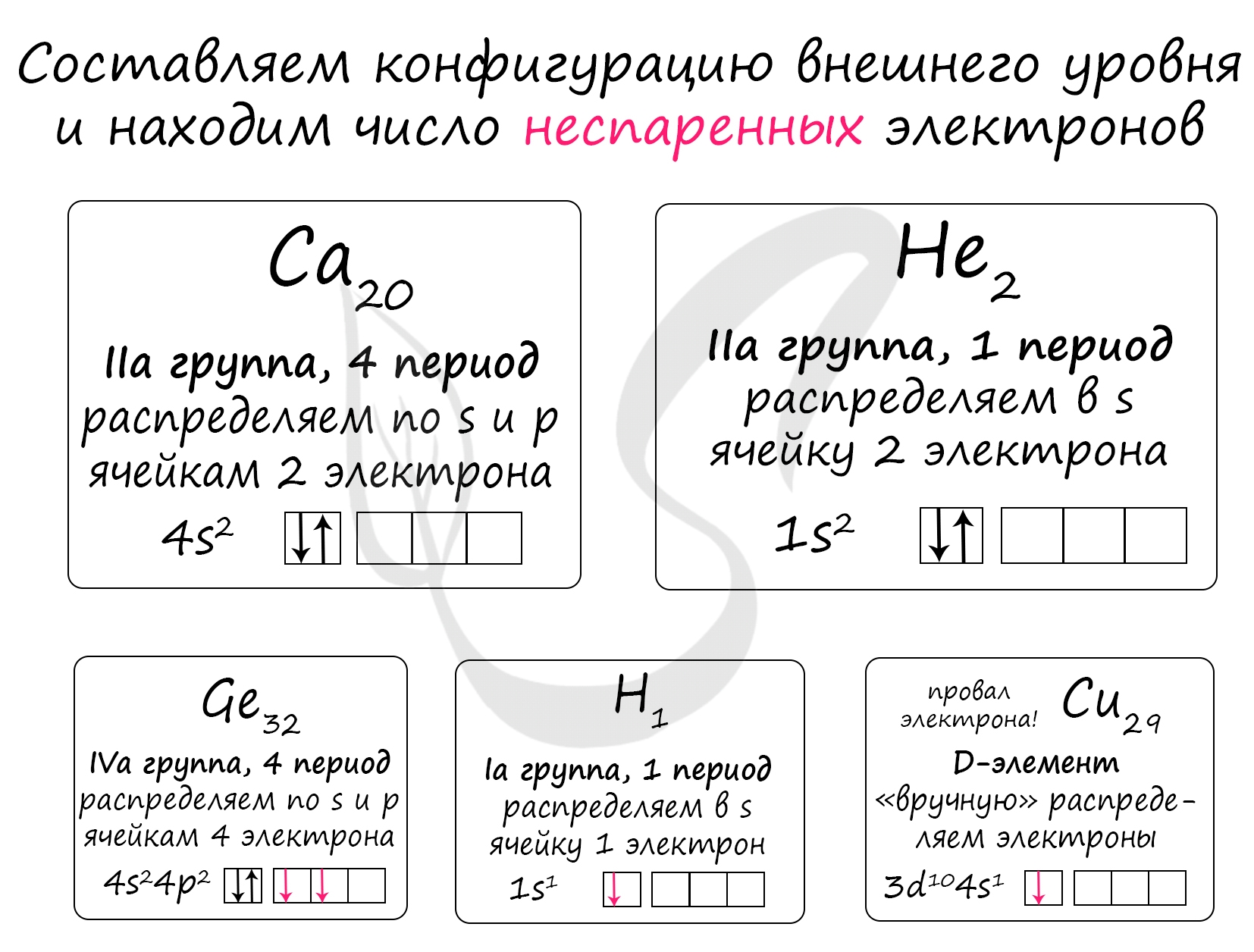
Выбранные элементы находятся в одном и том же периоде - 4. В периоде увеличение радиуса атома происходит справа налево (←), поскольку чем меньше электронов на внешнем уровне, тем радиус атома БОЛЬШЕ: электроны меньше притягиваются друг к другу и чувствуют себя более свободно :)
Радиус атома увеличивается: Ge (1) → Cu (5) → Ca (2)
Германий (1) имеет 4 электрона на внешнем уровне (125 · 10 -12 м - радиус атома германия)
Медь (5) имеет на внешнем уровне 1 электрон (провал электрона у меди!), но вспомним про d-подуровень который под завязку забит десятью электронами → за счёт этого радиус атома получается даже меньше (145 · 10-12) чем у кальция (194 · 10 -12)
У кальция (2) 2 электрона на внешнем уровне, которые чувствуют себя максимально свободно + нет электронов на d-подуровне
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6923.
Верный ответ: 35
Образуют оксиды в степени окисления, равной +1
3) H - вода является самым известным оксидом водорода (H2O), также используют название "гидроксид водорода"
5) Cu - степени окисления +1 (Cu2O), +2 (CuO)
Остальные пункты:
1) Ge - образует оксиды в степени окисления +2 (GeO), +4 (GeO2)
2) Ca - образует оксиды в степени окисления +2 (CaO)
4) He - инертный (благородный) газ с 8 электронной внешней оболочкой (полностью заполнена), а значит он не вступает в реакции - оксиды не образует
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6924.
Верный ответ: 45
Химическая связь образована за счёт общих электронных пар - подразумевается ковалентная связь, образованная по механизму обобществления (обменному механизму), а не донорно-акцепторному
4) Cl2 - ковалентная неполярная связь между атомами (Cl-Cl), атомы имеют одинаковую электроотрицательность → связь неполярная, обменный механизм
5) H2O - ковалентные полярные связи (O-H), между атомами с разной электроотрицательностью → связь полярная, обменный механизм
Остальные пункты:
1) NaCl - ионная связь, образуется между атомами с большой разницей в электроотрицательности (чаще всего: типичный металл + типичный неметалл)
2) CaO - ионная связь, образуется между атомами с большой разницей в электроотрицательности (чаще всего: типичный металл + типичный неметалл)
3) Ca - металлическая связь (между атомами металла в чистом веществе)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7100.

Верный ответ: 826
Под цифрами:
1 - оксид железа (II) - проявляет основные свойства, соответствует основанию Fe(OH)2
2 - гидроксид хрома (III) - проявляет амфотерные свойства: реагирует как с кислотами, так и с основаниями
3 - оксид хрома (VI) - кислотный оксид, соответствует хромовой кислоте (H2CrO4)
4 - гидроксид кальция (II) - в рамках ЕГЭ гидроксид кальция считается растворимым сильным основание (щелочь), проявляет основные свойства: реагирует с кислотами
5 - фтороводородная кислота - слабая одноосновная кислота
6 - оксид марганца (IV) проявляет амфотерные свойства: реагирует как с кислотами, так и с основаниями
7 - азотистая кислота - слабая одноосновная кислота
8 - хлорноватая кислота - сильная одноосновная кислота
9 - гидроксид бария (II) - щелочь (растворимое основание), проявляет основные свойства: реагирует с кислотами
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7801.

1) серная кислота
2) сульфид аммония
3) сульфат калия
4) сероводородная кислота
5) сульфит натрия
Верный ответ: 15
Cероводородная кислота (4) нам не подходит, так как это слабый электролит и её нельзя раскладывать на ионы. Не выбираем также сульфид (2) и сульфат (3), так как по условию задания мы должны выбрать сульфит.
Вещество X - H2SO4 (1)
Вещество Y - Na2SO3 (5)
В результате реакции серной кислоты с сульфитом натрия → образуется сульфат натрия и слабая неустойчивая сернистая кислота, которая сразу же распадается на воду и сернистый газ
Na2SO3 + H2SO4 = Na2SO4 + H2O + SO2↑
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7663.
Верный ответ: 4254
В этом задании скрыты 60 реакций! Правильный подход к его выполнению может значительно повысить ваш уровень знаний неорганической химии.
Итак, ключевой момент: нужно попробовать составить реакцию каждого из веществ (А, Б, В, Г) со всеми предложенными реагентами! Вы должны узнать, возможна ли каждая из этих реакций, или понять причину, по которой она невозможна (например, в реакции не может быть два осадка: и справа, и слева). Следуйте такому подходу, и вы удивитесь, как быстро повысится ваш "неорганический уровень" ;)
Реакции для Cr2O3 протекают так:
Cr2O3 + 2KOH = (t°) 2KCrO2 + H2O
Cr2O3 + 3SO3 = Cr2(SO4)3
Cr2O3 + 6HNO3 = 2Cr(NO3)3 + 3H2O
Реакции для FeCl2 протекают так:
FeCl2 + 2KOH = Fe(OH)2 + 2KCl
FeCl2 + 2NH3 + 2H2O = Fe(OH)2 + 2NH4Cl
FeCl2 + 2AgNO3 = Fe(NO3)2 + 2AgCl
Реакции для O2 протекают так:
O2 + 2K2SO3 = 2K2SO4
O2 + 2CO = 2CO2
O2 + 2NO = 2NO2
Реакции для Al(OH)3 протекают так:
Al(OH)3 + KOH = K[Al(OH)4]
2Al(OH)3 + 3SO3 = Al2(SO4)3 + 3H2O
Al(OH)3 + 3HNO3 = Al(NO3)3 + 3H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6964.
Верный ответ: 4625
А) Концентрированная азотная кислота является сильным окислителем, в реакции с солью (сульфат железа (II)) будет происходить окисление железа +2 до железа +3, с выделением побочного газообразного продукта, который характерен для концентрированной азотной кислоты - это оксид азота (IV)
FeSO4 + 4HNO3(конц.) = NO2 + H2SO4 + Fe(NO3)3 + H2O
Б) Разбавленная серная кислота ведёт себя как самая обычная кислота (например соляная), и здесь будет вытеснение водорода цинком, так как цинк стоит в ряду напряжения металлов левее водорода (цинк более активен, чем водород)
Zn + H2SO4 = ZnSO4(разб.) + H2
В) Пероксид водорода является сильным окислителем, поэтому произойдёт окисление йодида (-1) до йода (0),
калий в присутствии сульфат-ионов образует сульфат калия
H2O2 + H2SO4 + 2KI = K2SO4 + 2H2O + I2
Г) В присутствии пары сильных окислителей железо +2 будет окислено до железа +3, а хром примет наиболее устойчивую для него его степень окисления +3 (куда хром - туда и калий, поэтому калий также образует сульфат)
6FeSO4 + K2Cr2O7 + 7H2SO4 = 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7280.
Верный ответ: 15
Вещество X - (1) - O2
При сгорании дисульфида железа (пирита) образуется оксид железа (III) и сернистый газ
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
Вещество Y - (5) - CO
Железная окалина - Fe3O4 - это смесь двух оксидов (оксид железа (II) и оксид железа (III)), поэтому фактически наше задание сводится к получению оксида железа (II). Сделать это можно восстановив часть оксида железа (III) до оксида железа (II) хорошим восстановителем, например угарным газом
3Fe2O3 + CO = 2Fe3O4 + CO2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6826.
Верный ответ: 1342
А) Вторичный амин (этилметиламин) - общая формула R-NH-R' (CnH2n+3N) - наличие NH группы (аминогруппы), связь азота с двумя атомами углерода
Б) Сложный эфир (метилацетат или метиловый эфир уксусной кислоты) - общая формула СnH2nO2 - наличие двойной связи между углеродом и кислородом, наличие связи R-O-R'
В) Нитроалканы (нитроэтан) - общая формула CnH2n+1NO2 - наличие нитрогруппы (NO2), которая связана с предельным углеводородным радикалом
Г) Аминокислоты (аланин) - общая формула H2N-CH(R)-COOH - наличие и аминогруппы, и карбоксильной группы в одной молекуле
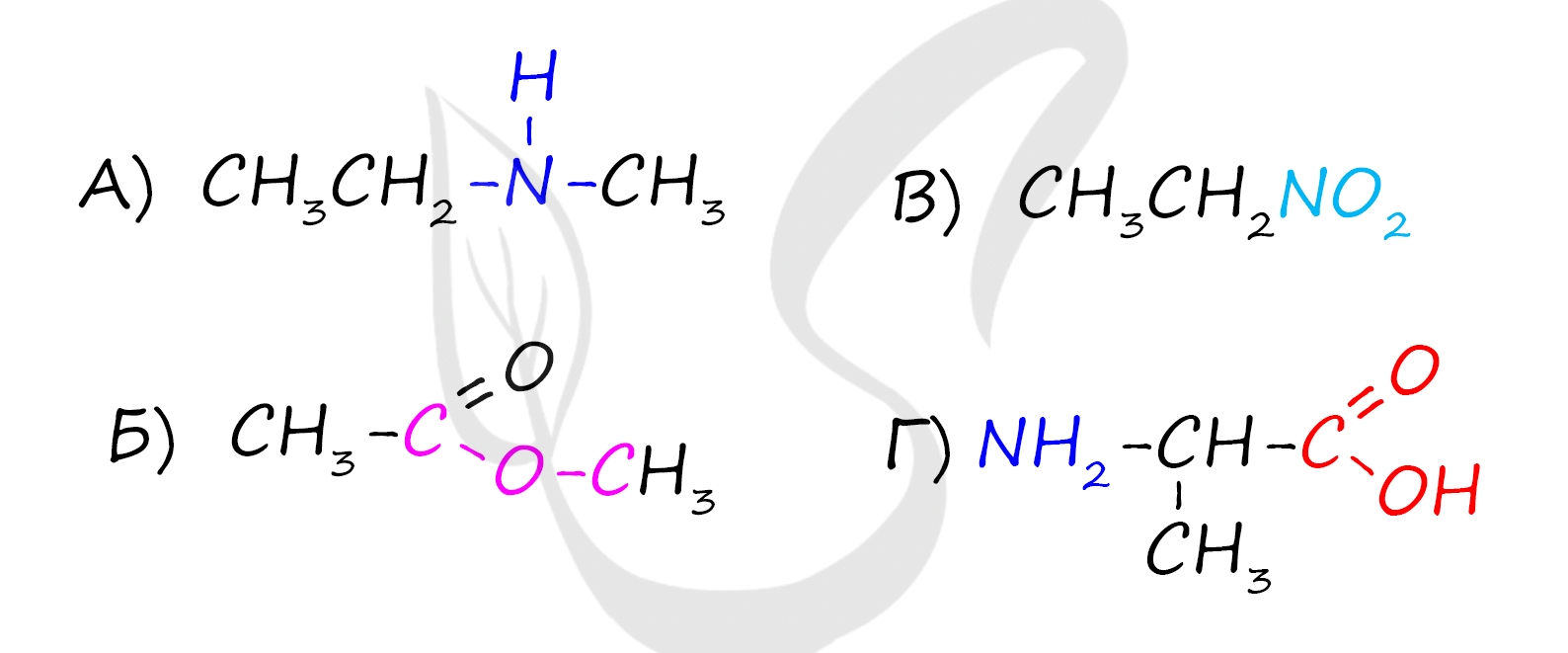
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7632.
Верный ответ: 34
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7878.
Верный ответ: 2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7704.
Верный ответ: 15
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7531.
Верный ответ: 4321
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7252.
Верный ответ: 6611
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6938.
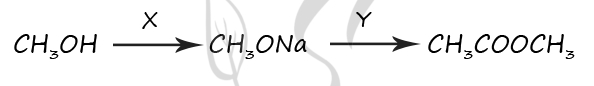
1) CH3COOH
2) CH3COONa
3) Na
4) Na2CO3
5) NaOH
6) CH3C(O)Cl
Верный ответ: 36
Для одноатомных спиртов не характерна реакция с NaOH (так как спирты - более слабые кислоты, чем вода, и образующиеся алкоголяты сразу подвергаются гидролизу), поэтому выбрать пункт 5 для первой реакции - ошибка.
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6904.
Верный ответ: 14
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7290.
Верный ответ: 15
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6801.
Верный ответ: 342
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7152.
Верный ответ: 5345
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6803.
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
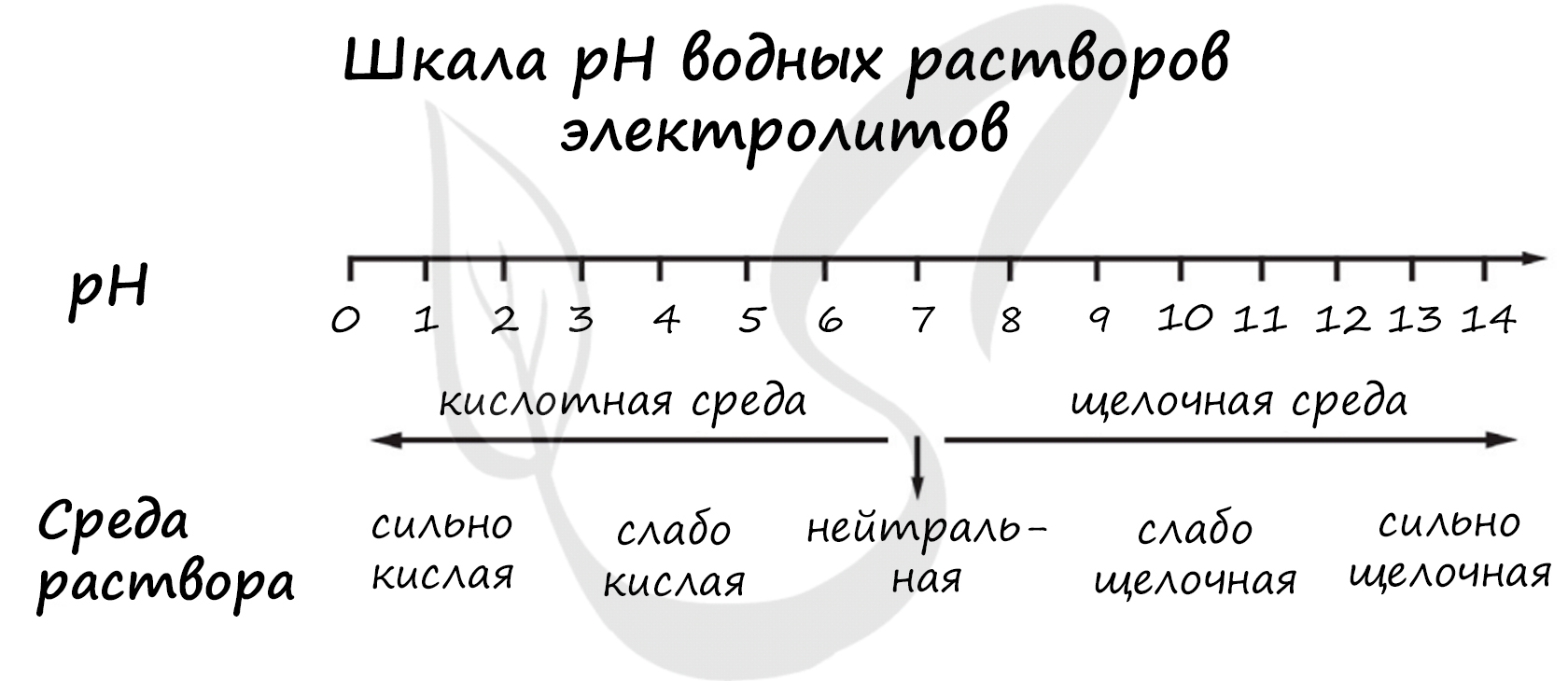
pH («пэ аш») - водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
1) NH4Cl
2) NH4HSO3
3) K2SO4
4) KHSO4
Верный ответ: 1243
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7924.
Верный ответ: 2313
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7855.
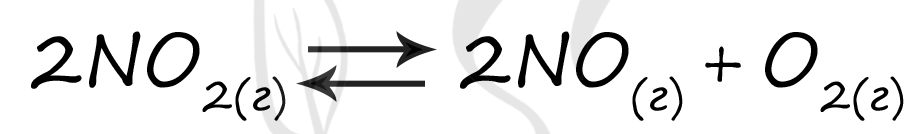
Верный ответ: 53
Таблица (по условиям задания)

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7207.
Верный ответ: 3343
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7576.
Верный ответ: 3214
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7367.
Ответом к заданиям 26-28 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Единицы измерения физических величин указывать не нужно.
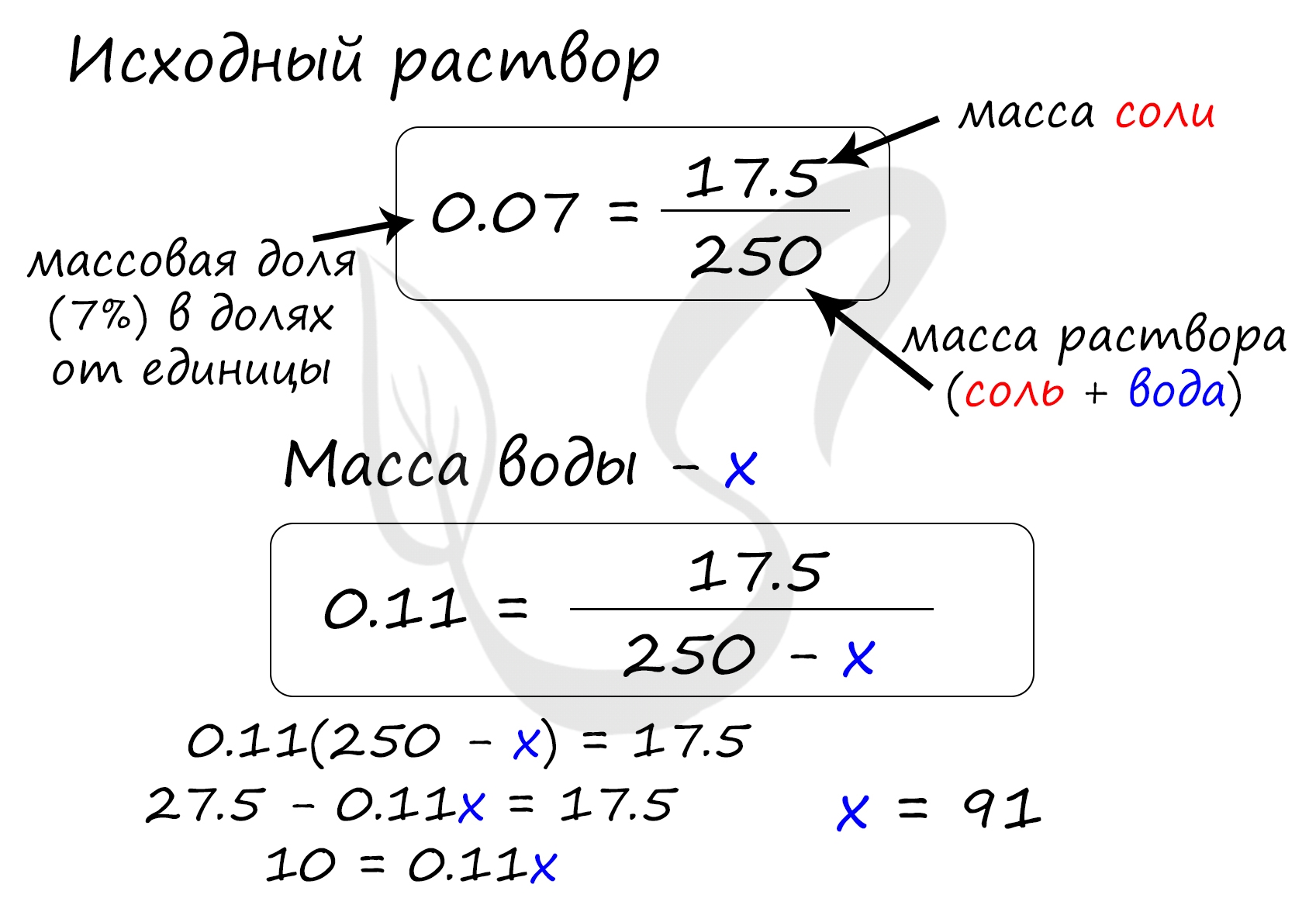
Верный ответ: 91
Найдем массу соли, которая присутствует в исходном растворе:
m(соли) = 250 · 0.07 = 17.5 грамм
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7158.
Верный ответ: 120

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7614.
Верный ответ: 44
CaCO3 + 2HNO3 = Ca(NO3)2 + CO2↑ + H2O
1) m(HNO3) = m · w = 220,5 · 0,2 = 44,1 кг
2) n(HNO3) = m / Mr = 44,1 кг / 63 кг/кмоль = 0,7 кмоль
3) n(CaCO3) = 1/2 · n(HNO3) = 1/2 · 0,7 = 0,35 кмоль
4) m(CaCO3) = n · Mr = 0,35 кмоль · 100 кг/кмоль = 35 кг
5) w(CaCO3) = 35 кг / 62,5 кг · 100% = 56%
6) w(примесей) = 100% - 56% = 44%
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7580.
Часть 2 Вы проверяете сами. Все пояснения и подсказки к частям 1 и 2 обязательно будут даны по окончании теста.
Для выполнения заданий 29,30 используйте следующий перечень веществ:
гидроксид калия, оксид серы(VI), оксид марганца(IV), хлорид алюминия, хлор. Допустимо использование водных растворов веществ.
Возможна следующая реакция:
MnO2 + Cl2 + 4KOH = K2MnO4 + 2KCl + 2H2O

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7651.

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7652.
1) P (или P4) + O2 = P4O10 (или 2P2O5)
2) P4O10 + 6H2O = 4H3PO4 (или P2O5 + 3H2O = 2H3PO4)
3) 2H3PO4 + 3Ca(OH)2 = Ca3(PO4)2↓ + 6H2O
4) Ca3(PO4)2 + 3H2SO4 = 3CaSO4 + 2H3PO4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7338.
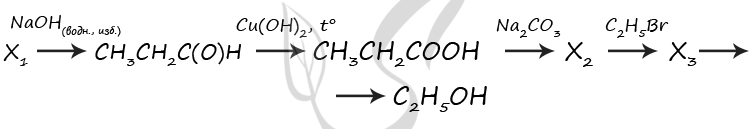
1) CH3-CH2-CHCl2 + 2NaOH = 2NaCl + H2O + CH3-CH2-C(O)H
2) CH3-CH2-C(O)H + 2Cu(OH)2 = (t°) CH3-CH2-COOH + Cu2O + 2H2O
3) 2CH3-CH2-COOH + Na2CO3 = 2CH3-CH2-COONa + CO2↑ + H2O
4) CH3-CH2-COONa + C2H5Br = CH3-CH2-COO-C2H5 + NaBr
5) CH3-CH2-COO-C2H5 + NaOH = (t°) CH3-CH2-COONa + C2H5OH
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6989.
1) Вычислим количества веществ кислорода и водорода, их массу, сделаем проверку на кислород
n(CO2) = 6,05 : 22,4 = 0,27 моль
m(C) = 0,27 ⋅ 12 = 3,24 г
n(H2O) = 4,86 : 18 = 0,27 моль
n(H) = 0,54 моль
m(H) = 0,54 ⋅ 1 = 0,54 г
m(C) + m(H) = 3,24 + 0,54 = 3,78 (кислород отсутствует)
Соотношение атомов: C : H = 0,24 : 0,54 = 1 : 2
Простейшая формула: CH2
Молярная масса вещества: M = 40 ⋅ 2,1 = 84 г
Молекулярная формула: C6H12
2) Структурная формула
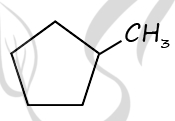

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6956.
1) Уравнения реакций
Al2O3 + 6HCl = 2AlCl3 + 3H2O (1)
Al2S3 + 6HCl = 2AlCl3 + 3H2S↑ (2)
H2S + CuSO4 = CuS↓ + H2SO4 (3)
2) Вычислим количество Al2O3
m(CuSO4) = 240 ⋅ 0,2 = 48 г
n(CuSO4) = 48 : 160 = 0,3 моль
n(CuSO4) = n(H2S) = 0,3 моль (по уравнению 3)
n(Al2S3) = 1/3 ⋅ n(H2S) = 1/3 ⋅ 0,3 = 0,1 моль (по уравнению 2)
m(Al2S3) = 0,1 ⋅ 150 = 15 г
n(Al)в Al2S3 = n(Al2S3) ⋅ 2 = 0,1 ⋅ 2 = 0,2 моль
m(Al)в Al2S3 = 0,2 ⋅ 27 = 5,4 г
Примем x = n(Al2O3)
n(Al)в Al2O3 = n(Al) ⋅ 2 = 2x моль
m(Al2O3) = x ⋅ 102 = 102x (г)
m(Al)в Al2O3 = 2x ⋅ 27 = 54x (г)
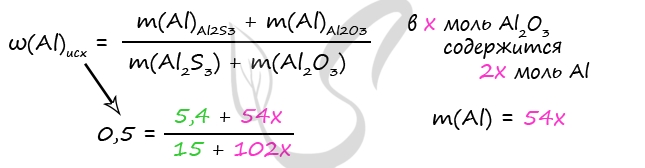

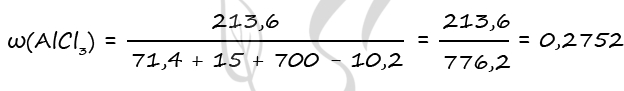
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7935.