


Для выполнения заданий 1-3 используйте следующий ряд химических элементов:
Ответом в заданиях 1-3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Верный ответ: 24
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7482.
Верный ответ: 431
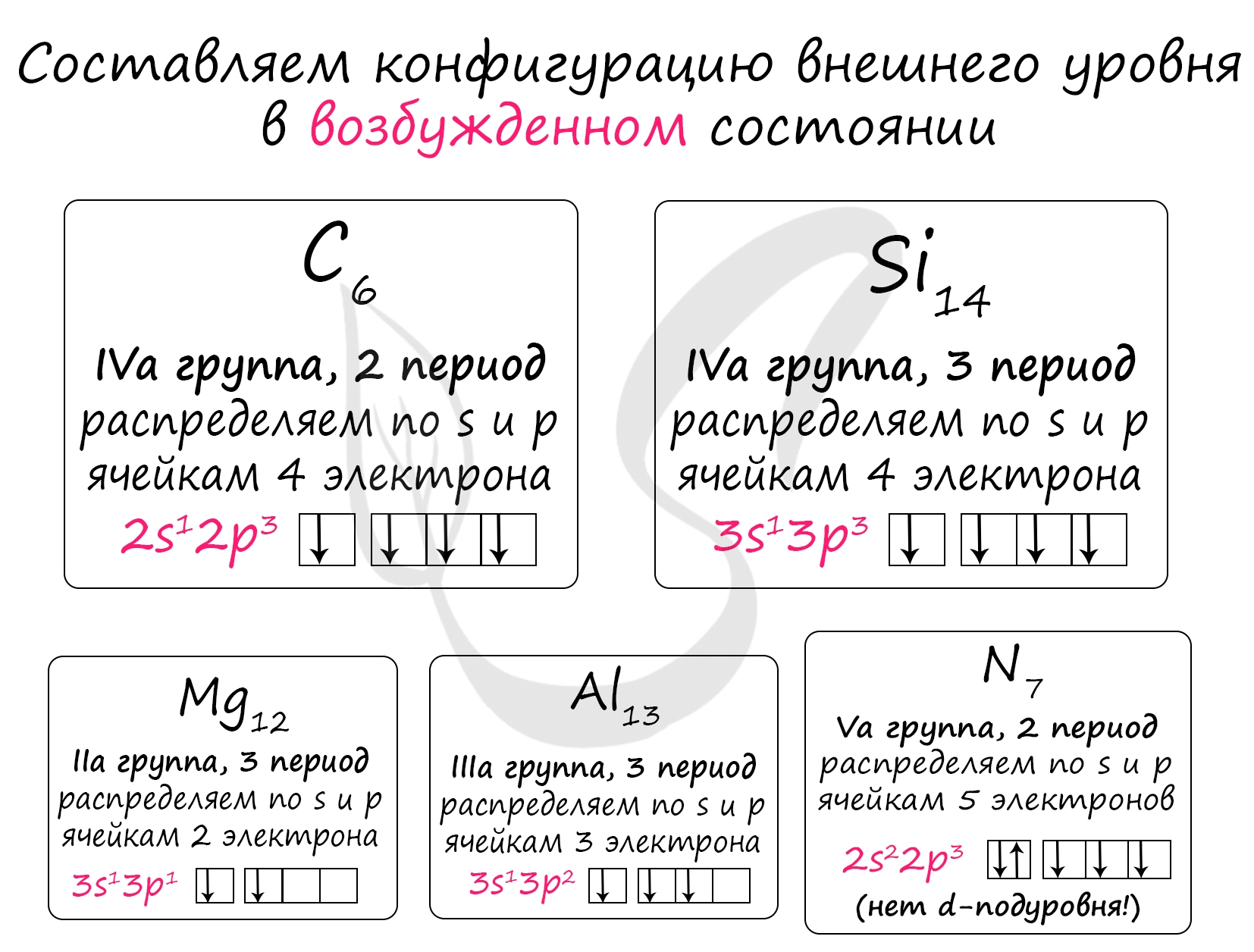
Выбранные элементы находятся в одном и том же периоде - 3, в периоде электроотрицательность уменьшается справа налево (← - по направлению от F)
Располагаем все элементы в порядке возрастания их электроотрицательности: Si (4) → Al (3) → Mg (1)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7483.
Верный ответ: 13
Проявляют постоянную степень окисления:
1) Mg - постоянная степень окисления +2 (MgO)
3) Al - постоянная степень окисления +3 (Al2O3)
Остальные пункты:
2) C - все степени окисления от -4 (CH4) до +4 (CO2)
4) Si - степени окисления -4 (силицид - Al4Si3), +2 (SiO), +4 (SiO2)
5) N - все степени окисления от -3 (NH3, Li3N) до +5 (HNO3, N2O5)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7484.
Верный ответ: 34
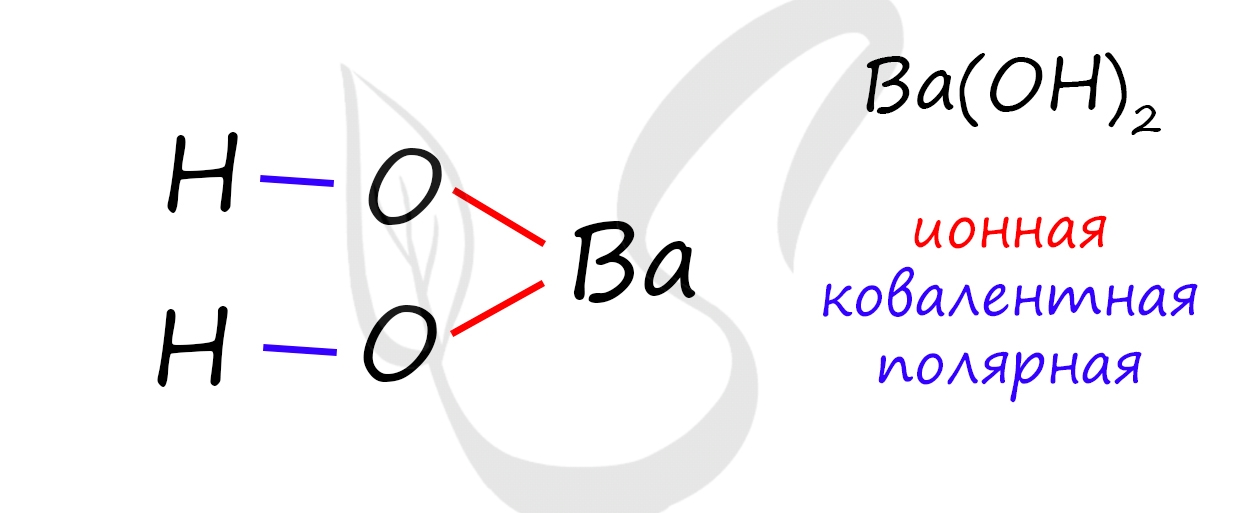
Как ионная, так и ковалентная химическая связь присутствуют в
3) Ba(OH)2 - гидроксид бария, между катионами Ba2+ и анионом OH- формируется ионная связь, а внутри аниона OH-, между H и O находится ковалентная полярная связь
4) NH4Cl - ионная связь, образуется между ионом NH4+ и ионом Cl-, а внутри катиона NH4+ между N и H находятся ковалентные полярные связи
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7240.

Верный ответ: 947
Под цифрами:
1 - фосфин (фосфид водорода, так как фосфор проявляет в фосфине степень окисления -3)
2 - основной карбонат свинца, основная соль (наличие гидроксид-ионов)
3 - тетрагидроксохромат(III) лития - комплексная соль (узнаем по наличию комплексного иона в квадратных скобках)
4 - дигидроортофосфат аммония, кислая соль ортофосфорной кислоты (H3PO4), слабой трехосновной кислоты
5 - бромид-йодид кальция (II) - смешанная соль (два аниона)
6 - нитрид натрия, бинарное неорганическое соединение металла натрия и азота
7 - сульфат железа-аммония (II), двойная соль (два катиона)
8 - озонид натрия
9 - бромид аммония, соль сильной соляной кислоты HBr
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7696.
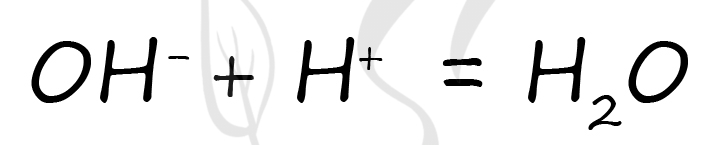
1) серная кислота
2) гидроксид бария
3) сульфид калия
4) угольная кислота
5) гидроксид натрия
Верный ответ: 51
Гидроксид бария (2) нам не подходит, так как по итогу реакции образуется нерастворимый сульфат бария. Сульфид калия (3) нам не подходит, так как по итогу реакции образуется газ - сероводород. А осадков или газов в сокращённом ионном уравнении мы не видим.
Вещество X - NaOH (5)
Вещество Y - H2SO4 (1)
В результате реакции обмена между гидроксидом натрия и серной кислотой → образуется растворимый сульфат натрия и вода
2NaOH + H2SO4 = 2H2O + Na2SO4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7488.
Верный ответ: 1325
В этом задании скрыты 60 реакций! Правильный подход к его выполнению может значительно повысить ваш уровень знаний неорганической химии.
Итак, ключевой момент: нужно попробовать составить реакцию каждого из веществ (А, Б, В, Г) со всеми предложенными реагентами! Вы должны узнать, возможна ли каждая из этих реакций, или понять причину, по которой она невозможна (например, в реакции не может быть два осадка: и справа, и слева). Следуйте такому подходу, и вы удивитесь, как быстро повысится ваш "неорганический уровень" ;)
Реакции для SO2 протекают так:
SO2 + CaO = CaSO3
SO2 + 2KOH = K2SO3 + H2O
2SO2 + O2 = 2SO3
Реакции для Ba(OH)2 протекают так:
Ba(OH)2 + K2SO4 = BaSO4 + 2KOH
3Ba(OH)2 + P2O5 = Ba3(PO4)2 + 3H2O
Ba(OH)2 + 2HNO3 = Ba(NO3)2 + 2H2O
Реакции для ZnI2 протекают так:
ZnI2 + H2SO4 = ZnSO4 + 2HI
ZnI2 + Na2CO3 = ZnCO3 + 2NaI
ZnI2 + 2LiOH = 2LiI + Zn(OH)2
Реакции для Ca протекают так:
2Ca + 2C2H5OH = 2C2H5OCa + H2
Ca + 2HCl = CaCl2 + H2
3Ca + N2 = Ca3N2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6999.
Верный ответ: 2221
А) Считать ли эту реакцию окислительно-восстановительный спорный вопрос: с одной стороны серная концентрированная кислота проявляет окислительные свойства и может окислить сульфит натрия до сульфата, но с другой стороны - здесь идёт обычная реакция обмена; в любом случае итоговая запись реакции сомнений не вызывает и записывается точно так же как пункт Б
Na2SO3 + H2SO4 = Na2SO4 + H2O + SO2
Б) Разбавленная серная кислота проявляет обычные кислотные свойства - не является окислителем, поэтому эта реакция будет идти по типу обмена, без изменения степеней окисления
Na2SO3 + H2SO4 = Na2SO4 + H2O + SO2
В) Концентрированная серная кислота проявляет окислительные свойства → под её действием сульфид натрия окисляется до сульфата натрия
Na2S + 4H2SO4 = Na2SO4 + 4H2O + 4SO2
Г) Разбавленная серная кислота проявляет обычные кислотные свойства - не является окислителем, поэтому эта реакция будет идти по типу обмена, без изменения степеней окисления
Na2S + H2SO4 = Na2SO4 + H2S
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7420.
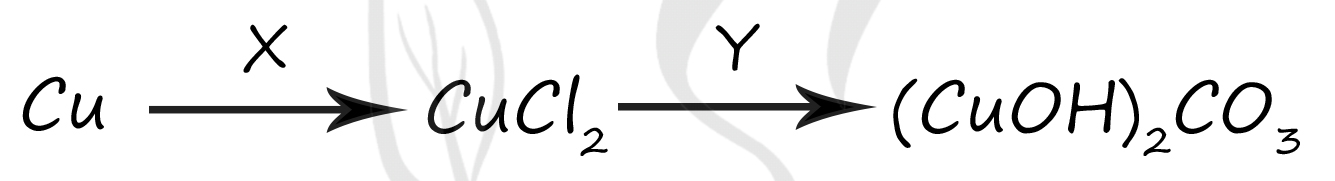
1) HCl
2) FeCl3
3) FeCl2
4) K2CO3
5) CaCO3
Верный ответ: 24
Вещество X - (2) - FeCl3
Медь не может вытеснить железо, это не реакция замещения; данная реакция идет, так как хлорид железа (III) обладает окислительными свойствами и способен окислить медь до хлорида меди (II)
Cu + FeCl3 = FeCl2 + CuCl2
Вещество Y - (4) - K2CO3
Вторая реакция идёт по известному типу реакций двойного гидролиза: однако гидроксид меди (II) в данном случае не просто выпадает в осадок, а реагирует с углекислым газом с образованием основной соли - карбоната гидроксомеди (II)
2CuCl2 + 2K2CO3 + H2O = (CuOH)2CO3 + 4KCl + CO2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6861.
Верный ответ: 3411
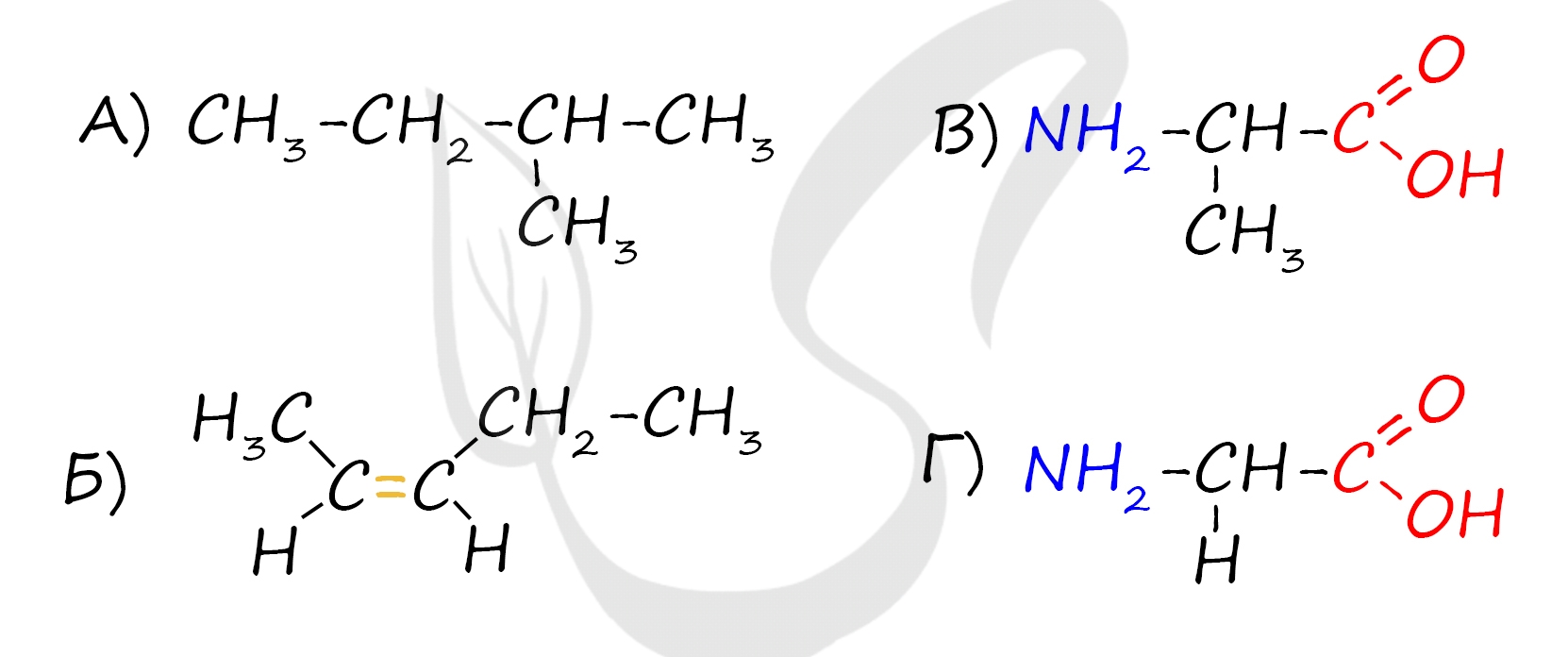
А) Алканы (изопентан) - общая формула CnH2n+2 - насыщенные (предельные) углеводороды, нет двойных/тройных связей
Б) Алкены (цис-пентен-2) - общая формула CnH2n - наличие одной двойной связи
(В) и (Г) Аминокислоты (аланин (2-аминопропановая кислота) и глицин) - общая формула H2N-CH(R)-COOH - наличие и аминогруппы, и карбоксильной группы в одной молекуле
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7387.
Верный ответ: 13
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7843.
Верный ответ: 3
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7249.
Верный ответ: 45
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7496.
Верный ответ: 1514
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7742.
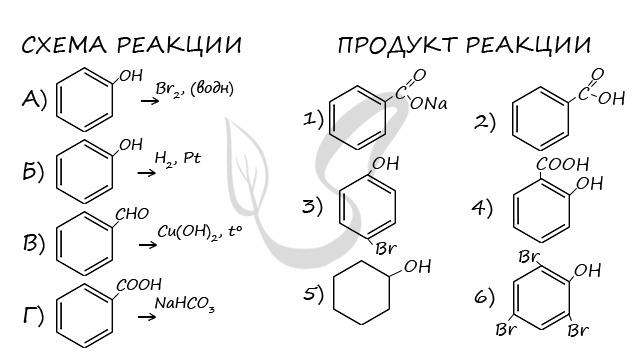
Верный ответ: 6521
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7498.
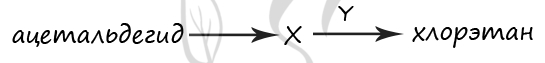
1) этан
2) ацетилен
3) хлороводород
4) этанол
5) хлор
Верный ответ: 43
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7394.
Верный ответ: 14
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7535.
Верный ответ: 25
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7746.
Верный ответ: 1422
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7397.
Верный ответ: 3111
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7293.
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
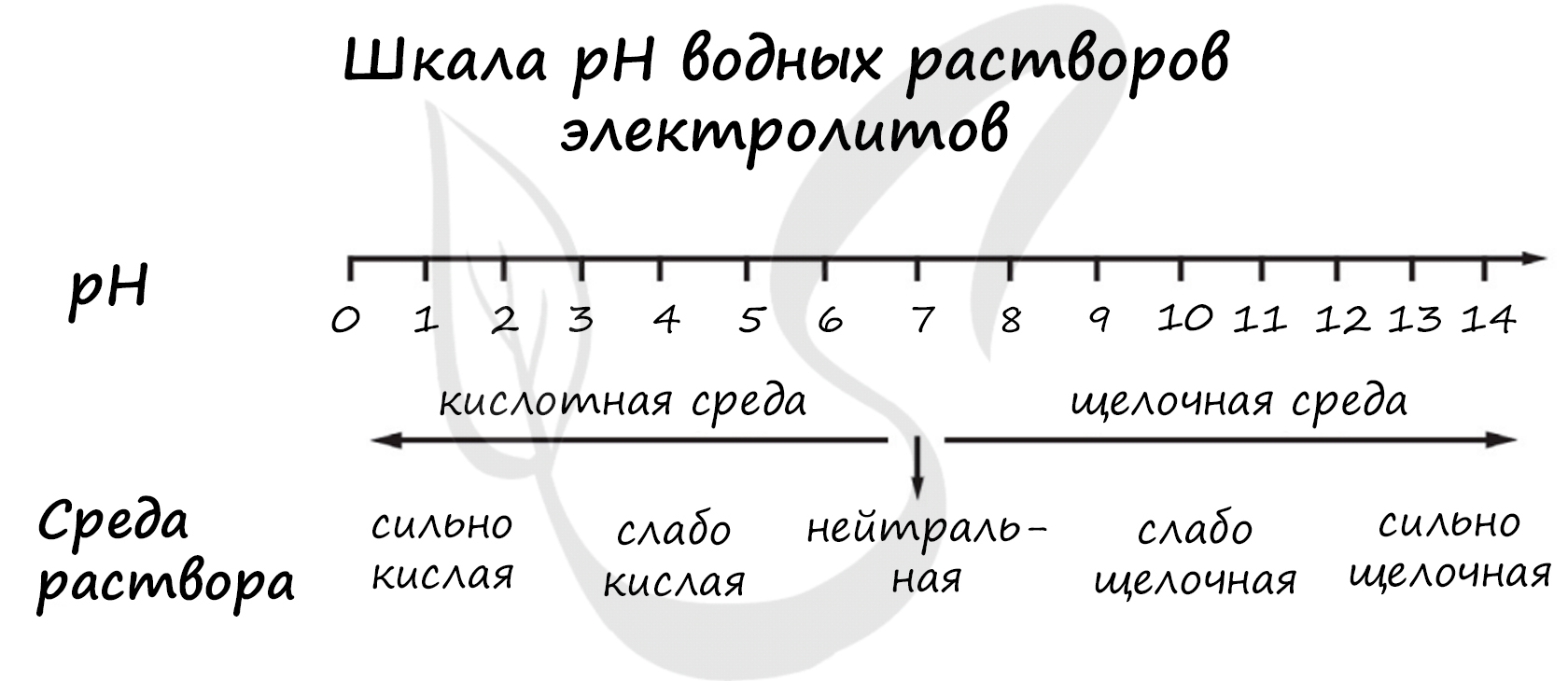
pH («пэ аш») - водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
1) HClO3
2) (CH3COO)2Ba
3) KNO3
4) AlBr3
Верный ответ: 1432
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6909.
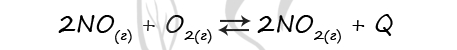
Верный ответ: 2212
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7505.
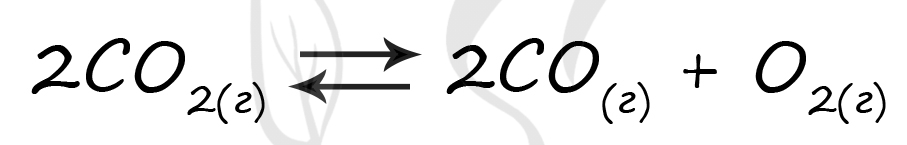
Верный ответ: 56
Таблица (по условиям задания)

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7452.
Верный ответ: 1112
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6981.
Верный ответ: 342
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7647.
Ответом к заданиям 26-28 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Единицы измерения физических величин указывать не нужно.
Верный ответ: 18,5
Вычислим массы первого и второго растворов:
m(р-ра)1 = 45 + 15 = 60 г
m(р-ра)2 = 65 + 10 = 75 г

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7788.
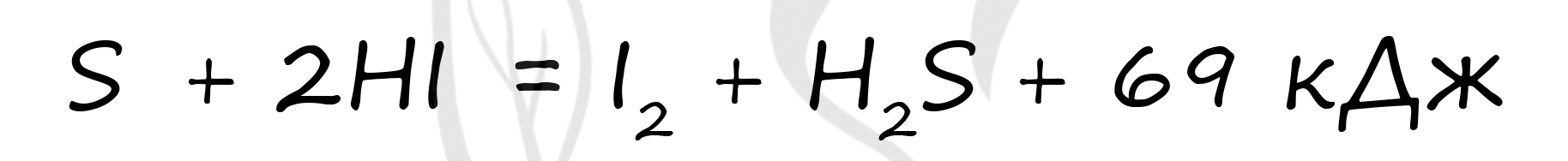
Верный ответ: 512

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7334.
Верный ответ: 75,6
(NH4)2Cr2O7 = Cr2O3 + N2↑ + 4H2O
Оксид элемента побочной подгруппы - есть не что иное, как оксид хрома (III) - Cr2O3
1) n(Cr2O3) = m / Mr = 136,8 г / 152 г/моль = 0,9 моль
2) n((NH4)2Cr2O7) = n(Cr2O3) = 0,9 моль
3) m((NH4)2Cr2O7) = n · Mr = 0,9 моль · 252 г/моль = 226,8 г
4) w((NH4)2Cr2O7) = 226,8 г / 300 г · 100% = 75,6%
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7510.
Часть 2 Вы проверяете сами. Все пояснения и подсказки к частям 1 и 2 обязательно будут даны по окончании теста.
Для выполнения заданий 29,30 используйте следующий перечень веществ:
нитрат алюминия, хлорид бария, бром, сульфат натрия, гидроксид калия. Допустимо использование водных растворов веществ.
Возможна следующая реакция:
3Br2 + 6KOH = KBrO3 + 5KBr + 3H2O

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7091.

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7092.
1) BaCl2 + Na2SO4 = BaSO4 + 2NaCl
2) NaCl + H2SO4(конц.) = NaHSO4 + HCl
(или 2NaCl + H2SO4 = Na2SO4 + 2HCl)
3) 8HCl + Fe3O4 = 2FeCl3 + FeCl2 + 4H2O
4) 5FeCl2 + KMnO4 + 8HCl = 5FeCl3 + KCl + MnCl2 + 4H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7688.
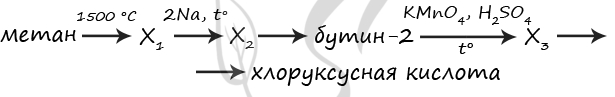
1) 2CH4 = (1500 °C) CH≡CH + 3H2
2) CH≡CH + 2Na = (t°) Na-C≡C-Na + H2
3) Na-C≡C-Na + 2CH3I = CH3-C≡C-CH3 + 2NaI
4) 5CH3-C≡C-CH3 + 6KMnO4 + 9H2SO4 = (t°) 10CH3COOH + 6MnSO4 + 3K2SO4 + 4H2O
5) CH3COOH + Cl2 = (P) Cl-CH2-COOH + HCl
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7689.
Общая формула амина - СxHyNz
1) Найдены количества вещества продуктов сгорания и определена молекулярная формула вещества:
n(CO2) = 2,69 : 22,4 = 0,12 моль
n(C) = 0,12 моль
n(H2O) = 3,24 : 18 = 0,18 моль
n(H) = 0,18 ⋅ 2 = 0,36 моль
m(N) = 2,36 - 0,12 ⋅ 12 - 0,36 = 0,56 г
n(N) = 0,56 : 14 = 0,04 моль
Соотношение: x : y : z = 0,12 : 0,36 : 0,04 = 3 : 9 : 1
Молекулярная формула исходного амина: C3H9N
2) Структурная формула вещества:
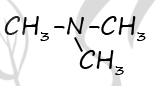
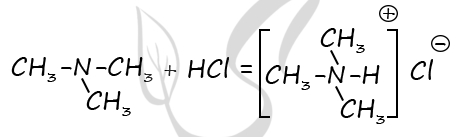
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7201.
1) Уравнения реакций
2LiCl + 2H2O = 2LiOH + H2 + Cl2
Cl2 + 2FeCl2 = 2FeCl3
2) Рассчитаем количество веществ хлорида лития, хлора и массу хлорида железа (II)
m(LiCl) = 31,875 ⋅ 0,08 = 2,55 г
n(LiCl) = 2,55 : 42,5 = 0,06 моль
n(Cl2) = 0,5n(LiCl) = 0,03 моль
n(FeCl2) = n(FeCl3) = 2n(Cl2) = 0,06 моль
3) Вычислим массу раствора и массовую долю хлорида железа (II) в растворе
m(FeCl2) = 0,06 ⋅ 127 = 7,62 г
mр-ра(FeCl2) = mр-ра(FeCl3) - m(Cl2)
mр-ра(FeCl3) = m(FeCl3) : ω(FeCl3) = 0,06 ⋅ 162,5 : 0,13 = 75 г
mр-ра(FeCl2) = 75 - 0,03 ⋅ 71 = 72,87 г
ω(FeCl2) = 7,62 : 72,87 ⋅ 100% = 10,46%
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7130.