


Для выполнения заданий 1-3 используйте следующий ряд химических элементов:
Ответом в заданиях 1-3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
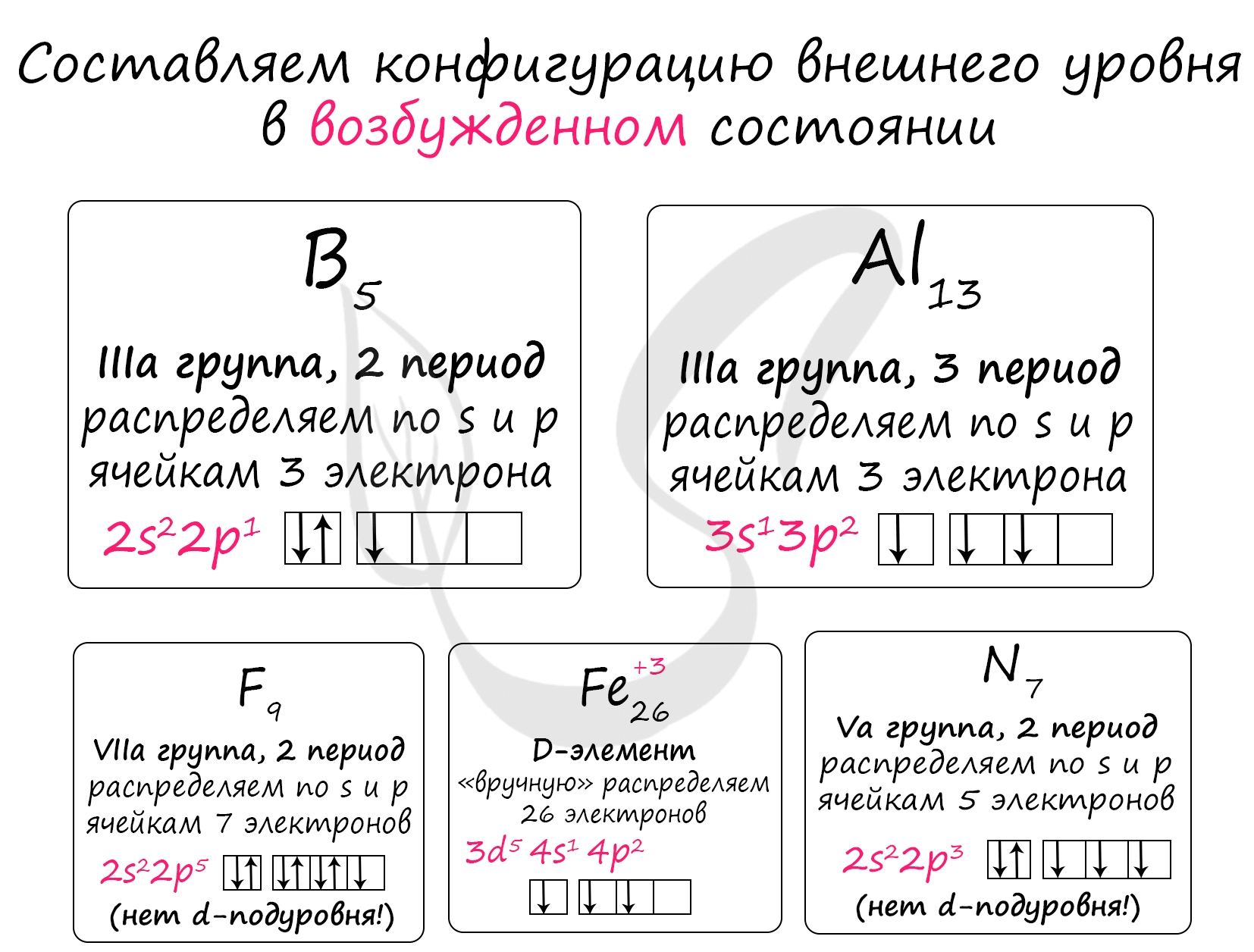
Верный ответ: 34
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7517.
Верный ответ: 153
Выбранные элементы находятся в одном и том же периоде - 2. В периоде электроотрицательность уменьшается справа налево (← - по направлению от F)
Располагаем все элементы в порядке уменьшения их электроотрицательности: F (1) → N (5) → B (3)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7518.
Верный ответ: 25
Проявляют в оксидах степень окисления как +2, так и +3:
2) Fe - степени окисления +2 (FeO), +3 (Fe2O3), +6 (Na2FeO4)
5) N - все степени окисления от -3 (NH3, Li3N) до +5 (HNO3, N2O5), в том числе +2 (NO) + 3 (N2O3)
Остальные пункты:
1) F - постоянная степень окисления -1 (HF)
3) B - степень окисления -3 (бориды - Mg3B2), +3 (B2O3, H3BO3)
4) Al - постоянная степень окисления +3 (Al2O3)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7519.
Верный ответ: 45
Химические связи, образованные по донорно-акцепторному механизму, присутствуют в
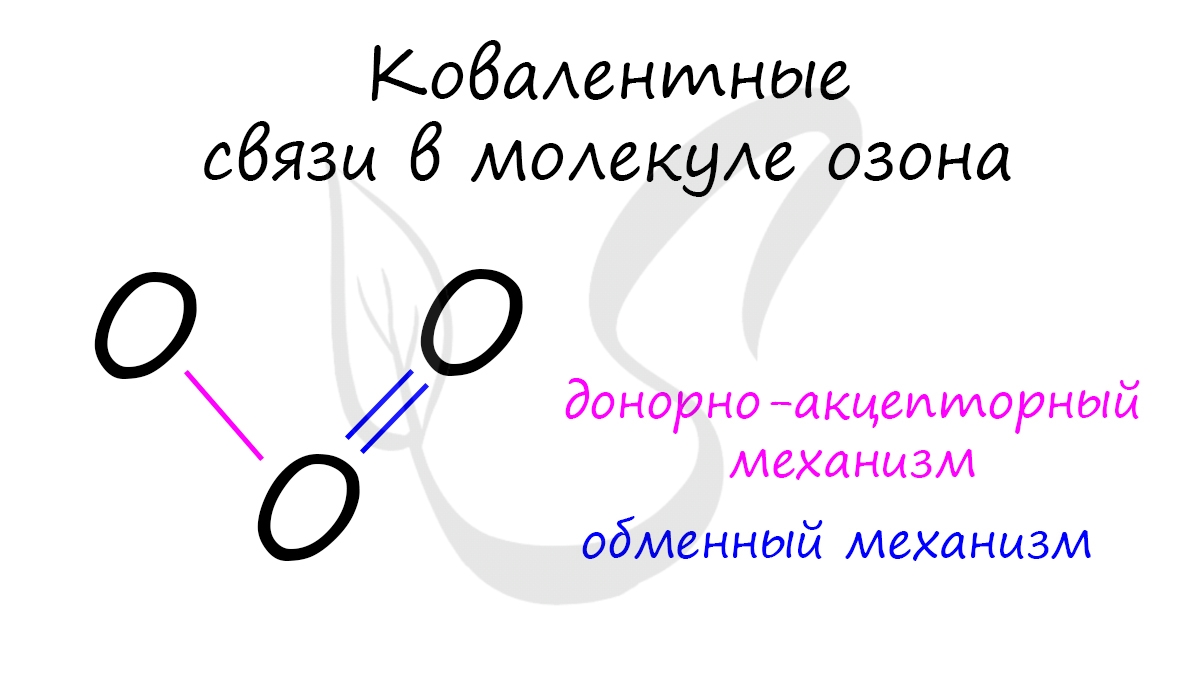
4) O3 - озон (строение ниже на рисунке)
5) HNO3 - в нитрат ионе [NO3]- есть ковалентная связь, образованная по донорно-акцепторному механизму
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6890.

Верный ответ: 916
Под цифрами:
1 - йодистая кислота - HIO2, записанная максимально хитро =) слабая одноосновная кислота
2 - ортофосфорная кислота, является трехосновной кислотой, так в ее составе присутствуют три атома водорода, которые она может отдать в реакции с основанием
3 - нитрид натрия, бинарное неорганическое соединение металла натрия и азота
4 - боран (гидрид бора)
5 - метаалюминиевая кислота (метаалюминат) - HAlO2, неустойчивая слабая кислота
6 - дихромовая кислота H2Cr2O7, записанная так, чтобы запутать и сбить нас с толку; сильная двухосновная кислота (имеет два протона, которые может отдать при диссоциации)
7 - оксихлорид фосфора
8 - гидроксохлорид железа (II), основная соль (наличие гидроксид-ионов)
9 - гидроксид калия - щелочь (растворимое основание), проявляет основные свойства: реагирует с кислотами
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7241.

1) Cu(OH)2
2) Al(NO3)3
3) (OH)3PO
4) Ba(OH)2
5) AlPO4
Верный ответ: 24
Вещество X - Al(NO3)3 (2)
Вещество Y - Ba(OH)2 (4)
Вещества под цифрами 1 и 5 сразу отсекаем, так как они нерастворимы и на ионы, как указано в условии, их разложить невозможно.
В варианте 3 просто нет необходимости - зачем нам ортофосфорная кислота?)
Мы должны выбрать именно растворимые вещества, которые диссоциируют на ионы
2Al(NO3)3 + 3Ba(OH)2 = 2Al(OH)3↓ + 3Ba(NO3)2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7033.
Верный ответ: 1435
В этом задании скрыты 60 реакций! Правильный подход к его выполнению может значительно повысить ваш уровень знаний неорганической химии.
Итак, ключевой момент: нужно попробовать составить реакцию каждого из веществ (А, Б, В, Г) со всеми предложенными реагентами! Вы должны узнать, возможна ли каждая из этих реакций, или понять причину, по которой она невозможна (например, в реакции не может быть два осадка: и справа, и слева). Следуйте такому подходу, и вы удивитесь, как быстро повысится ваш "неорганический уровень" ;)
Реакции для H3PO4 протекают так:
3Ca + 2H3PO4 = Ca3(PO4)2 + 3H2
3MgO + 2H3PO4 = Mg3(PO4)2 + 3H2O
H3PO4 + 3NH3 = (NH4)3PO4
Реакции для KOH протекают так:
N2O5 + 2KOH = 2KNO3 + H2O
3Cl2 + 6KOH = (t°) 5KCl + KClO3 + 3H2O
3KOH + H3PO4 = K3PO4 + 3H2O
Реакции для CO протекают так:
Fe3O4 + 4CO = 3Fe + 4CO2
CO + 2H2 = CH3OH
2CO + O2 = 2CO2
Реакции для Al2O3 протекают так:
Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O
Al2O3 + 2NaOH = 2NaAlO2 + H2O
Al2O3 + K2O = 2KAlO2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7874.
Верный ответ: 1133
А) Обычная реакция обмена, происходит без изменения степеней окисления
K2S + 2HCl = 2KCl + H2S
Б) Обычная реакция обмена, происходит без изменения степеней окисления
KHS + HCl = KCl + H2S
В) Обычная реакция обмена, происходит без изменения степеней окисления, образующаяся сернистая кислота (H2SO3) сразу же распадается на воду и SO2
KHSO3 + HCl = KCl + SO2 + H2O
Г) Обычная реакция обмена, происходит без изменения степеней окисления, образующаяся сернистая кислота (H2SO3) сразу же распадается на воду и SO2
2HCl + K2SO3 = 2KCl + H2O + SO2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7735.

1) ZnS
2) Zn3(PO4)2
3) CO2
4) ZnCl2
5) H2
Верный ответ: 54
Вещество X - (5) - H2
Водород является хорошим восстановителем, который восстанавливает цинк из оксида цинка (II)
ZnO + H2 = Zn + H2O
Вещество Y - (4) - ZnCl2
В реакции цинка с соляной кислотой цинк проявляет себя как более активный металл, стоящий в ряду напряжения левее водорода, и вытесняет водород из кислоты
Zn + 2HCl = ZnCl2 + H2↑
Однако почему не подходят сульфид цинка (1) или фосфат цинка (2)? Они являются нерастворимыми соединениями, а в самой последней реакции получается тоже нерастворимое соединение - гидроксид цинка (II). Нельзя из одного нерастворимого вещества (из одного осадка) получить другое нерастворимое вещество (другой осадок), поэтому в предпоследней реакции мы стараемся образовать именно какую-то растворимую соль цинка - идеально нам подходит хлорид цинка (II).
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7841.
Верный ответ: 3254
А) Начинаем нумерацию углеродной цепи от атома углерода, который входит в карбоксильную группу → 3-аминопропановая кислота
Б) Начинаем нумерацию углеродной цепи от атома углерода, который входит в карбоксильную группу → 2-аминопропановая кислота
В) Молекула симметрична → начинать нумерацию углеродной цепи можно от любого краевого атома углерода → бутин-2
Г) Молекула ассиметрична → начинаем нумерацию от краевого атома углерода, к которому прилежит тройная связь → бутин-1
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7422.
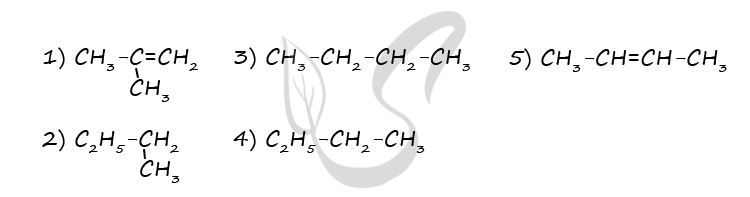
Верный ответ: 15
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7388.
Верный ответ: 134
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7389.
Верный ответ: 15
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6796.
Верный ответ: 5412
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7637.
Верный ответ: 1365
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6763.
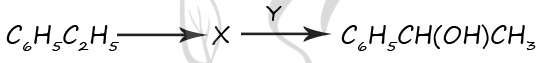
1) гидроксид калия (водный раствор)
2) α-хлорэтилбензол
3) бензол
4) толуол
5) гидроксид калия (спиртовой раствор)
Верный ответ: 21
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7289.
Верный ответ: 13
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7605.
Верный ответ: 35
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7501.
Верный ответ: 142
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7012.
Верный ответ: 5244
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6943.
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») - водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
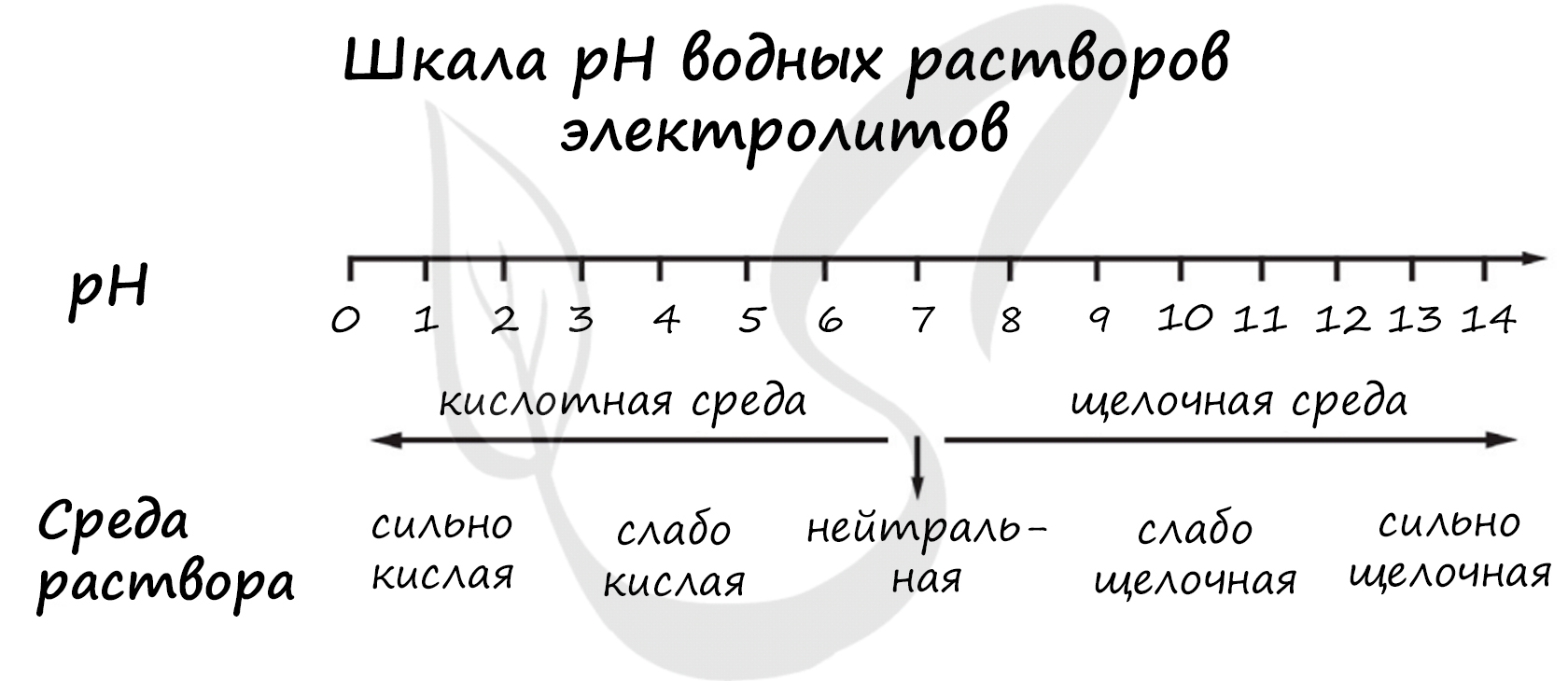
1) ZnSO4
2) H2Cr2O7
3) Na2S
4) KF
Верный ответ: 2143
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7609.

Верный ответ: 2231
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7820.

Верный ответ: 42
Таблица (по условиям задания)
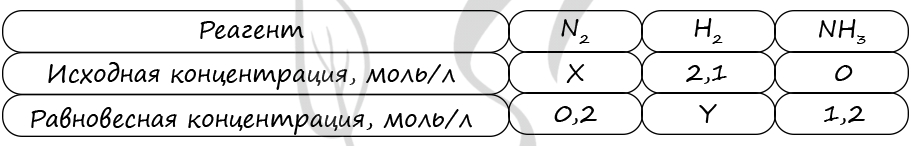
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7137.
Верный ответ: 4212
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7401.
Верный ответ: 112
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6912.
Ответом к заданиям 26-28 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Единицы измерения физических величин указывать не нужно.
Верный ответ: 30
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7858.

Верный ответ: 277
Исходя из реакции мы видим, что при участии 3 моль кислорода выделилось 830 кДж
По пропорции легко вычислить, что при участии 1 моль кислорода выделяется 277 кДж
3 моль - 830 кДж
1 моль - x кДж
x = 830 / 3 = 276,7 кДж (округляем до целых)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7369.
Верный ответ: 15
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7545.
Часть 2 Вы проверяете сами. Все пояснения и подсказки к частям 1 и 2 обязательно будут даны по окончании теста.
Для выполнения заданий 29,30 используйте следующий перечень веществ:
сульфат бария, хромат калия, ортофосфат натрия, сероводород, иодид лития. Допустимо использование водных растворов веществ.
Возможна следующая реакция:
2K2CrO4 + 3H2S + 2H2O = 2Cr(OH)3↓ + 3S↓ + 4KOH

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7301.

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7302.
1) CaC2 + 2H2O = (t°) Ca(OH)2 + C2H2↑
2) Cu2O + 4NH3 + H2O = 2[Cu(NH3)2]OH
3) C2H2 + 2[Cu(NH3)2]OH = Cu-C≡C-Cu↓ + 4NH3↑ + 2H2O
4) 3CuO + 2NH3 = (t°) 3Cu + N2 + 3H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7373.

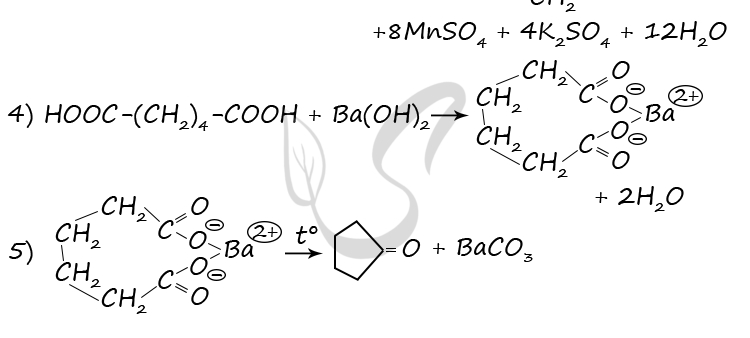
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6814.
1) Молярная масса углеводорода
M(CnH2n-6) = 27,6 : 0,3 = 92 г/моль
Установлена молекулярная формула ароматического углеводорода:
M(CnH2n-6) = 12n + 2n - 6 = 92
14n = 98
n = 7
Молекулярная формула - C7H8
2) Структурная формула метилциклогексана
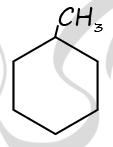
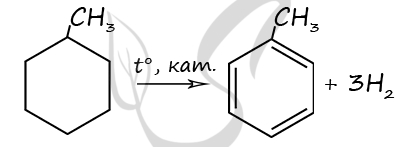
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7831.
1) Уравнения реакций
Na2S + 2H2O = 2NaOH + H2 + S
4NaOH + ZnSO4 = Na2[Zn(OH)4] + Na2SO4
2) Рассчитаем количество вещества гидроксида натрия и сульфата цинка
m(Na2S) = 100 ⋅ 0,078 = 7,8 г
n(Na2S) = 7,8 : 78 = 0,1 моль
n(NaOH) = 2n(Na2S) = 0,2 моль
n(ZnSO4) = n(ZnSO4⋅7H2O) = 5,74 : 287 = 0,02 моль
3) Очевидно, что гидроксид натрия в большом избытке, поэтому вторая реакция протекает с образованием комплексной соли. Максимальная масса осадка выпадет при нейтрализации остатка гидроксида натрия и частичном разрушении комплекса:
NaOH + HCl = NaCl + H2O
Na2[Zn(OH)4] + 2HCl = 2NaCl + Zn(OH)2 + 2H2O
n(NaOHост.) = 0,2 - 0,02 ⋅ 4 = 0,12 моль
n(Na2[Zn(OH)4]) = n(ZnSO4) = 0,02 моль
4) Вычислим массу 20%-го раствора соляной кислоты
n(HCl) = 2n(Na2[Zn(OH)4]) + n(NaOHост.) = 0,04 + 0,12 = 0,16 моль
m(HCl) = 0,16 ⋅ 36,5 = 5,84 г
mр-ра(HCl) = 5,84 : 0,2 = 29,2 г
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7270.