


Для выполнения заданий 1-3 используйте следующий ряд химических элементов:
Ответом в заданиях 1-3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Верный ответ: 23

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7412.
Верный ответ: 523
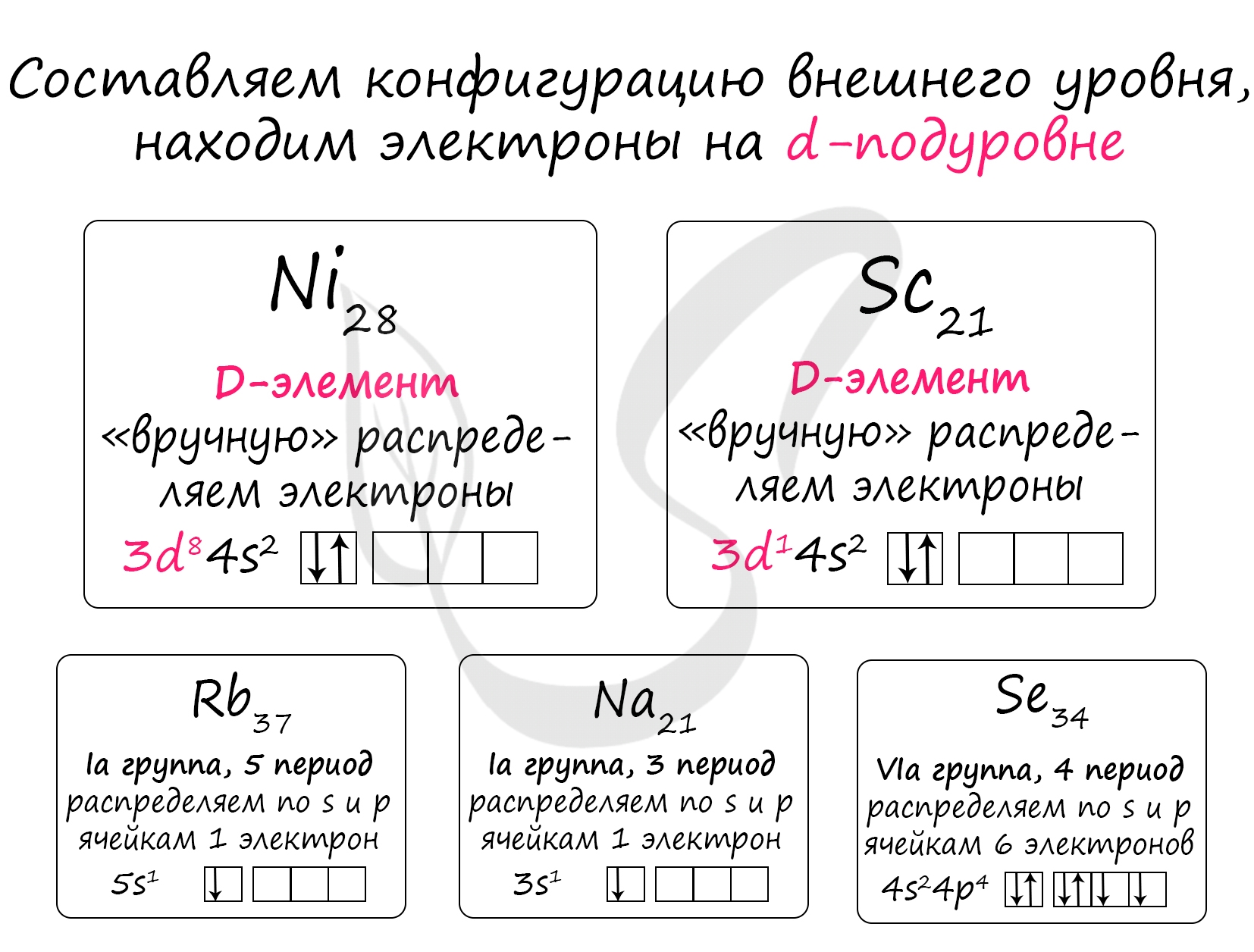
Выбранные элементы находятся в одном и том же периоде - 4. В периоде увеличение радиуса атома происходит справа налево (←), поскольку чем меньше электронов на внешнем уровне, тем радиус атома БОЛЬШЕ: электроны меньше притягиваются друг к другу и чувствуют себя более свободно :)
У селена на внешнем уровне 6 электронов (4s24p4) - ставим на 1 место в последовательности как наименьший радиус
Сравнивая между собой никель и скандий учитываем не только электроны внешнего уровня (их число одинаково и равно 2), но и электроны предвнешнего d-подуровня:
У никеля на внешнем уровне 2 электрона и на предвнешнем d-уровне 8 электронов (3d84s2)
У скандия на внешнем уровне 2 электрона и на предвнешнем d-уровне 1 электрон (3d14s2)
Радиус атома увеличивается: Se (5) → Ni (2) → Sc (3)
Точные академические данные по радиусам атома:
Se - 103 · 10-12
Ni - 149 · 10-12
Sc - 184 · 10-12
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7413.
Верный ответ: 14
Проявляют высшую степень окисления +1:
1) Rb - постоянная степень окисления +1
4) Na - постоянная степень окисления +1
Остальные пункты:
2) Ni - наиболее распространенные степени окисления +2 (NiO), но также есть +3 (Ni(OH)3), +4 (тетракарбонилникель - Ni(CO)4)
3) Sc - наиболее распространенная степень окисления +3 (Sc2O3), но есть также +1, +2
5) Se - степени окисления -2 (селениды - Na2Se), +4 (SeO2), +6 (SeO3)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7414.
Верный ответ: 35
Ионная химическая связь присутствует в
3) CsCl - ионная связь, образуется между атомами с большой разницей в электроотрицательности (чаще всего: типичный металл + типичный неметалл)
5) Rb2O - ионная связь, образуется между атомами с большой разницей в электроотрицательности (чаще всего: типичный металл + типичный неметалл)
Остальные пункты:
1) CO - ковалентные полярные связи (C-O), между атомами неметаллов с разной электроотрицательностью → связь полярная
2) H2SO4 - ковалентные полярные связи (H-O, S-O)
4) HCl - ковалентная полярная связь (H-Cl)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7870.

Верный ответ: 258
Под цифрами:
1 - аммиак - нитрид водорода (так как в аммиаке азот имеет степень окисления -3), считается слабым основанием, аммиак соединяется с кислотами с образованием солей аммония
2 - оксид натрия - проявляет основные свойства (степень окисления кислорода в оксидах -2, а натрия +1), соответствует основанию NaOH
3 - пероксид кальция (степень окисления кальция +2, а степень окисления кислорода в пероксидах -1)
4 - ацетат аммония, соль слабой уксусной кислоты CH3COOH
5 - угарный газ, оксид углерода (II) - несолеобразующий оксид
6 - бромид фосфора (V), высший бромид фосфора
7 - азотная кислота - сильная одноосновная кислота
8 - сернистая кислота, слабая двухосновная кислота
9 - оксид азота (III) - кислотный оксид, соответствует слабой одноосновной азотистой кислоте (HNO2)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7521.
1) аммиак
2) хлорид цинка
3) карбонат калия
4) хромат натрия
5) хлороводородная кислота
Верный ответ: 35
Вещество X - K2CO3 (3)
Вещество Y - HCl (5)
В результате реакции обмена между карбонатом калия и соляной кислотой → образуется хлорид калия и слабая угольная кислота, которая сразу же распадается на воду и углекислый газ
K2CO3 + 2HCl = H2O + 2KCl + CO2↑
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7313.
Верный ответ: 5433
В этом задании скрыты 60 реакций! Правильный подход к его выполнению может значительно повысить ваш уровень знаний неорганической химии.
Итак, ключевой момент: нужно попробовать составить реакцию каждого из веществ (А, Б, В, Г) со всеми предложенными реагентами! Вы должны узнать, возможна ли каждая из этих реакций, или понять причину, по которой она невозможна (например, в реакции не может быть два осадка: и справа, и слева). Следуйте такому подходу, и вы удивитесь, как быстро повысится ваш "неорганический уровень" ;)
Реакции для KI протекают так:
KI + AgNO3 = AgI + KNO3
6KI + 8HNO3= 2NO + 3I2 + 4H2O + 6KNO3
2KI + Cl2 = 2KCl + I2 (йод менее активный неметалл, чем хлор, поэтому хлор вытесняет йод)
Реакции для BaCO3 протекают так:
BaCO3 + 2HCl = BaCl2 + H2O + CO2
BaCO3 + 2CH3COOH = Ba(CH3COO)2 + H2O + CO2
BaCO3 + CO2 + H2O = Ba(HCO3)2
Реакции для HNO3 (разб.) протекают так:
2HNO3 + CaCO3 = Ca(NO3)2 + CO2 + H2O
2HNO3 + Ba(OH)2 = Ba(NO3)2 + 2H2O
HNO3 + KOH = KNO3 + H2O
Реакции для CO2 протекают так:
CaCO3 + H2O + CO2 = Ca(HCO3)2
Ba(OH)2 + CO2 = BaCO3 + H2O
CO2 + 2KOH = K2CO3 + H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7384.
Верный ответ: 4463
А) Основание + кислотный оксид: следует сохранить степени окисления цинка (+2) и серы (+6), поэтому в данной реакции образуется именно сульфат цинка (в сульфатах сера +6)
Zn(OH)2 + SO3 = ZnSO4 + H2O
Б) Реакция обмена между гидроксидом цинка и серной кислотой → приводит к образованию сульфата цинка и воды
H2SO4 + Zn(OH)2 = ZnSO4 + 2H2O
В) В расплаве образование комплексной соли невозможно, так как при столь высоких температурах испаряется вода → образуется смесь оксидов натрия и цинка - цинкат натрия
Zn(OH)2 + 2NaOH = (t°) Na2ZnO2 + 2H2O
Г) Гидроксид цинка обладает амфотерными свойствами - в реакции с гидроксидом натрия образуется комплексная соль
Zn(OH)2 + 2NaOH = Na2[Zn(OH)4] - тетрагидроксоцинкат натрия
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7630.
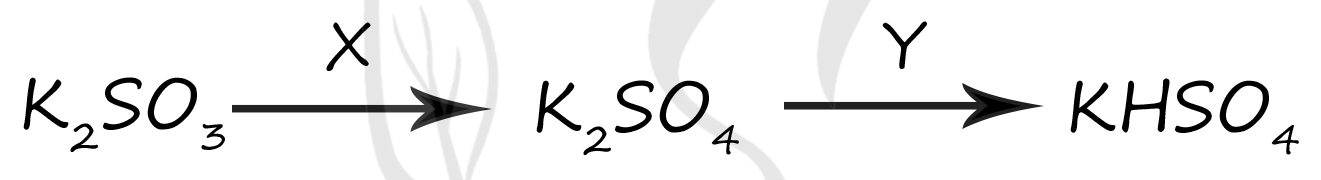
1) H2SO4
2) NaNO3(р-р)
3) SO2
4) NaOH
5) H2O2
Верный ответ: 51
Вещество X - (5) - H2O2
Чтобы получить из сульфита → сульфат, следует взять какой-нибудь окислитель - например пероксид водорода
K2SO3 + H2O2 = K2SO4 + H2O
Вещество Y - (1) - H2SO4
Чтобы получить из средней соли → кислую - следует добавить к средней соли соответствующую кислоту
K2SO4 + H2SO4 = 2KHSO4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7141.
Верный ответ: 3312
А) Сложный эфир (метилформиат) - общая формула СnH2nO2 - наличие двойной связи между углеродом и кислородом, наличие связи R-O-R'
Б) Нитроглицерин - сложный эфир трехатомного спирта глицерина и азотной кислоты
В) Глицерин - многоатомный (трехатомный) спирт - содержит 3 гидроксильных группы (OH группы)
Г) Аминокислоты (глицин) - общая формула H2N-CH(R)-COOH - наличие и аминогруппы, и карбоксильной группы в одной молекуле
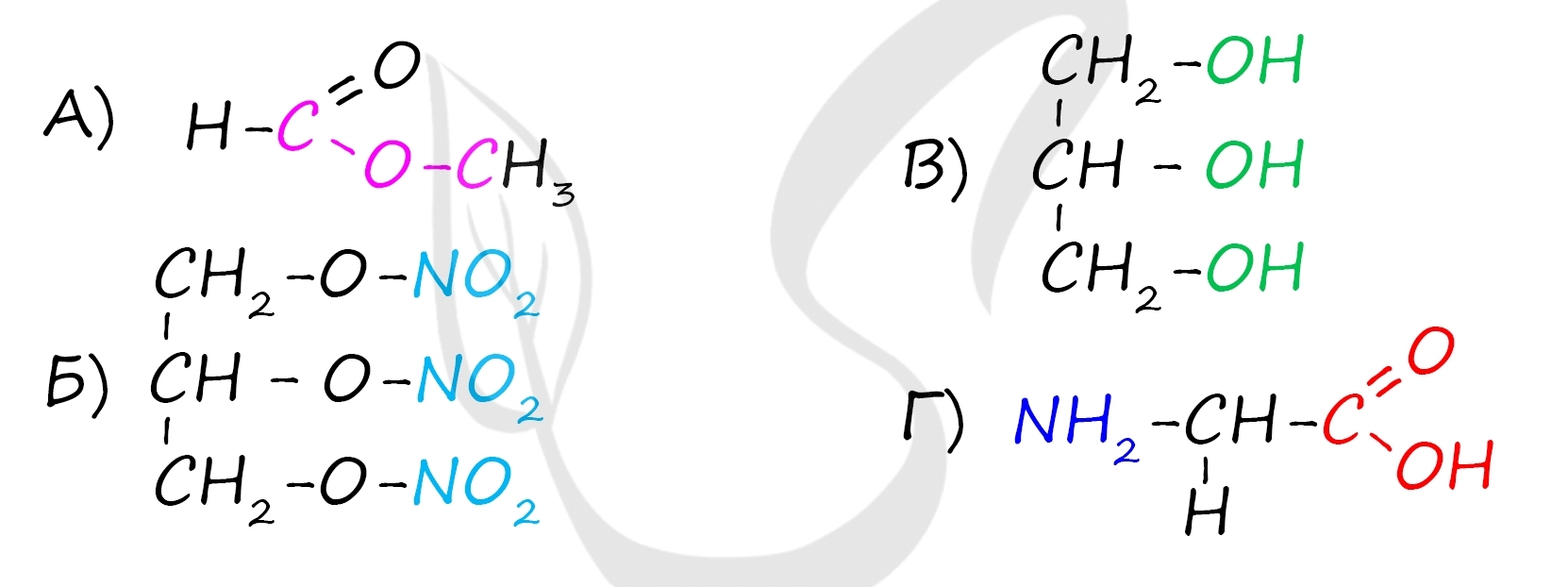
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7002.
Верный ответ: 14
Грубое простое (но крайне полезное! :) объяснение:
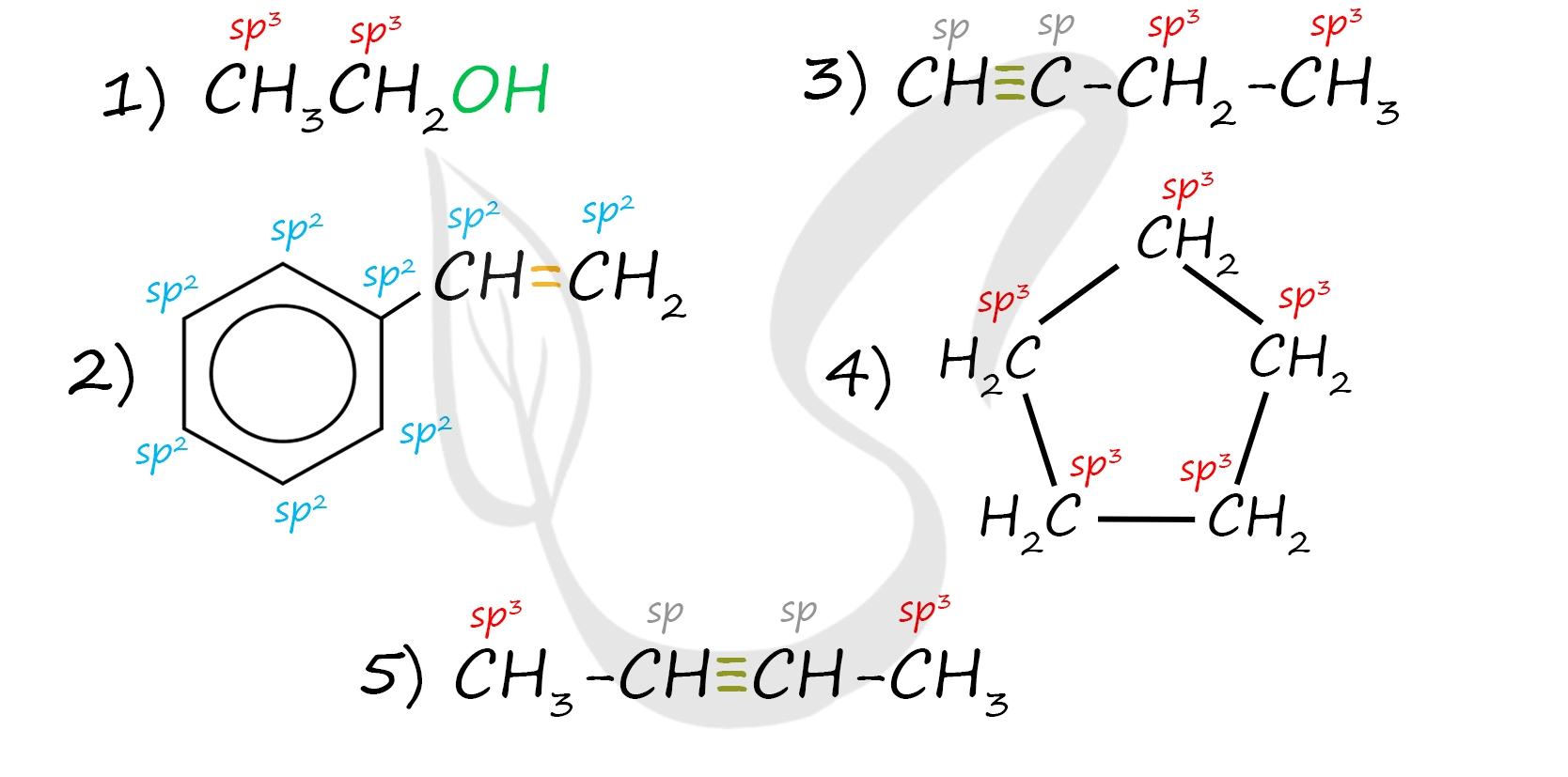
sp3-гибридизация - если атом углерода имеет только σ-связи (сигма-связи), например алканы и циклоалканы
sp2-гибридизация - если атом углерода имеет одну π-связь (пи-связь), например алкены
sp-гибридизация - если атом углерода имеет две π-связи (пи-связь), например алкины
В больших молекулах наблюдается сочетания разных по типу гибридизации атомов углерода:
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6758.
Верный ответ: 234
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7319.
Верный ответ: 34
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7111.
Верный ответ: 4224
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7882.
Верный ответ: 1653
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7638.
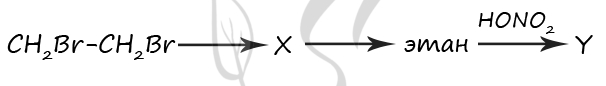
1) ацетилен
2) этиламин
3) этандиол
4) оксид углерода(IV)
5) нитроэтан
Верный ответ: 15
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6869.
Верный ответ: 25
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7115.
Верный ответ: 34
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6906.
Верный ответ: 412
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7817.
Верный ответ: 1243
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7853.
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») - водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
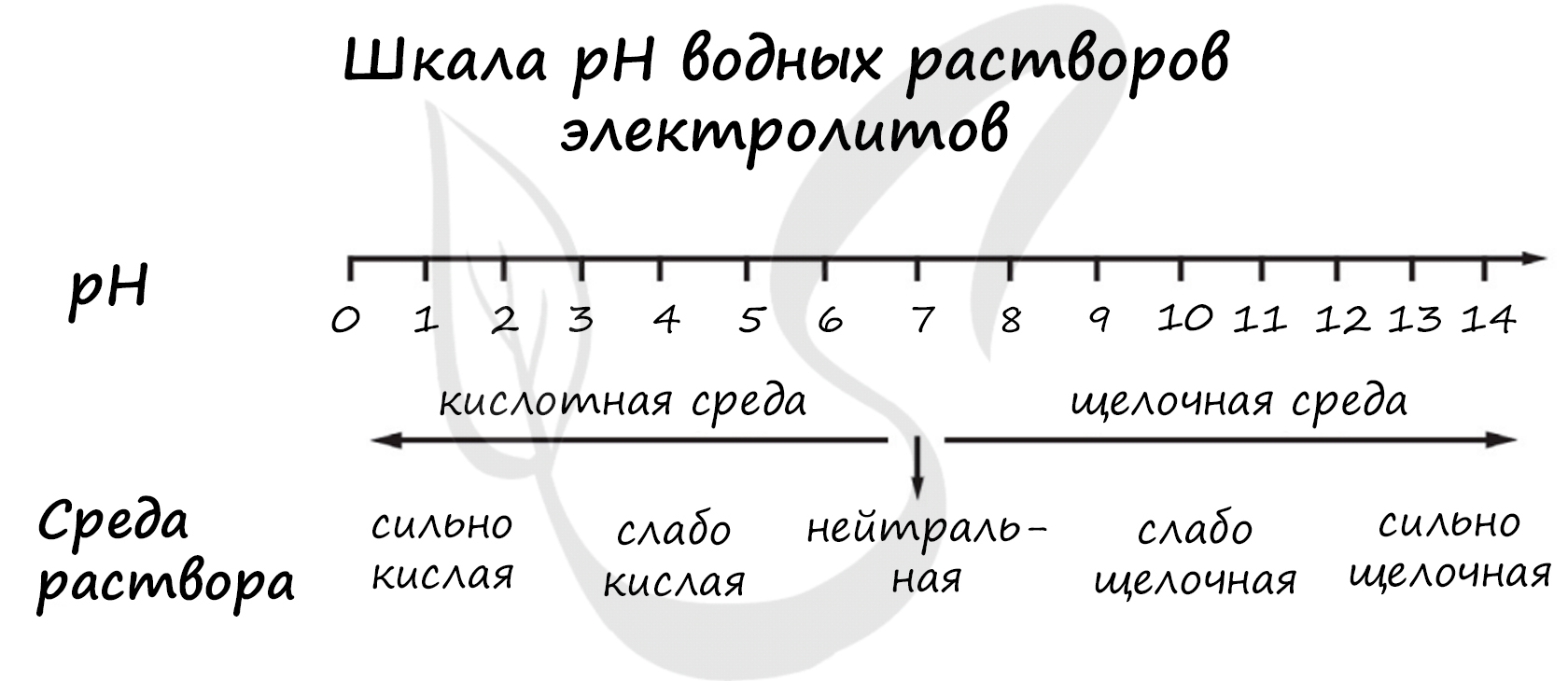
1) HI
2) SnBr2
3) Ca(NO2)2
4) KOH
Верный ответ: 1234
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7189.
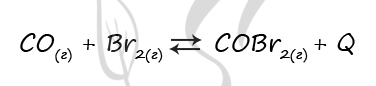
Верный ответ: 2121
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6945.
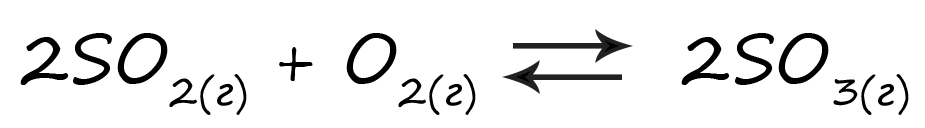
Верный ответ: 43
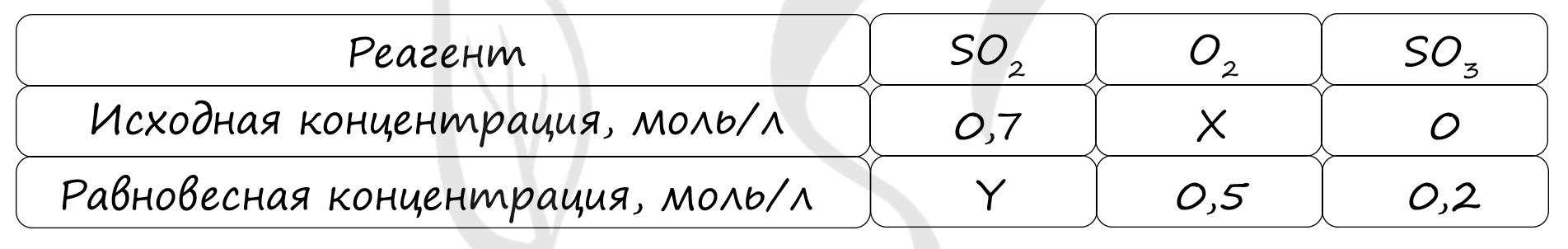
Таблица (по условию задачи)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7032.
Верный ответ: 1231
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7121.
Верный ответ: 134
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6982.
Ответом к заданиям 26-28 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Единицы измерения физических величин указывать не нужно.
Верный ответ: 133,3
Найдем массу соли, которая присутствует в исходном растворе:
m(соли) = 200 · 0.05 = 10 грамм

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6913.
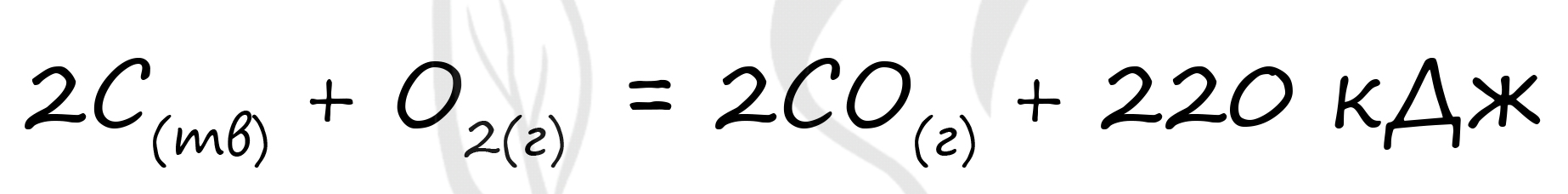
Верный ответ: 44

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7579.
Верный ответ: 87,5
2HCl + CaCO3 = CaCl2 + H2O + CO2↑
1) n(CO2) = v / Vr = 6,272 м3 / 22,4 м3/кмоль = 0,28 кмоль
2) n(CaCO3) = n(CO2) = 0,28 кмоль
3) m(CaCO3) = n · Mr = 0,28 кмоль · 100 кг/кмоль = 28 кг
4) w(CaCO3) = 28 кг / 32 кг · 100% = 87,5%
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7895.
Часть 2 Вы проверяете сами. Все пояснения и подсказки к частям 1 и 2 обязательно будут даны по окончании теста.
Для выполнения заданий 29,30 используйте следующий перечень веществ:
нитрит натрия, серная кислота, иодид натрия, гидроксид калия, нитрат магния. Допустимо использование водных растворов веществ.
Возможна следующая реакция:
2Nal + 2NaNO2 + 2H2SO4 = I2↓ + 2NO↑ + 2Na2SO4 + 2H2O

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6881.

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6882.
1) Ca3(PO4)2 + 3SiO2 + 5C = (t°) 3CaSiO3 + 2P + 5CO
2) 4P + 3KOH + 3H2O = (t°) PH3↑ + 3KH2PO2
3) PH3 + 8HNO3(конц.) = H3PO4 + 8NO2 + 4H2O
4) KH2PO2 + 2Br2 + 2H2O = H3PO4 + KBr + 3HBr
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6918.

1) CaC2 + 2H2O = Ca(OH)2 + CH≡CH↑
2) CH≡CH + H2O = (Hg2+, H2SO4, t°) CH3CHO
3) 5CH3CHO + 2KMnO4 + 3H2SO4 = 5CH3COOH + K2SO4 + 2MnSO4 + 3H2O
4) CH3COOH + Cl2 = (P) Cl-CH2-COOH + HCl
5) Cl-CH2-COOH + 2NH3 = NH2-CH2-COOH + NH4Cl
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7794.
1) Найдём соотношение атомов углерода, водорода и кислорода в молекуле органического соединения:
С : H : О = 60/12 : 13,3/1 : 26,7/16 = 5 : 13,3 : 1,67 = 3 : 8 : 1
Простейшая формула C3H8O
2) Структурная формула
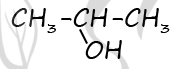

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7096.
1) Запишем реакцию
2AgNO3 + H2S = Ag2S↓ + 2HNO3
2) Определим массу раствора и массу растворенного нитрата серебра после охлаждения

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6780.