


Для выполнения заданий 1-3 используйте следующий ряд химических элементов:
Ответом в заданиях 1-3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Верный ответ: 35
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6747.
Верный ответ: 234
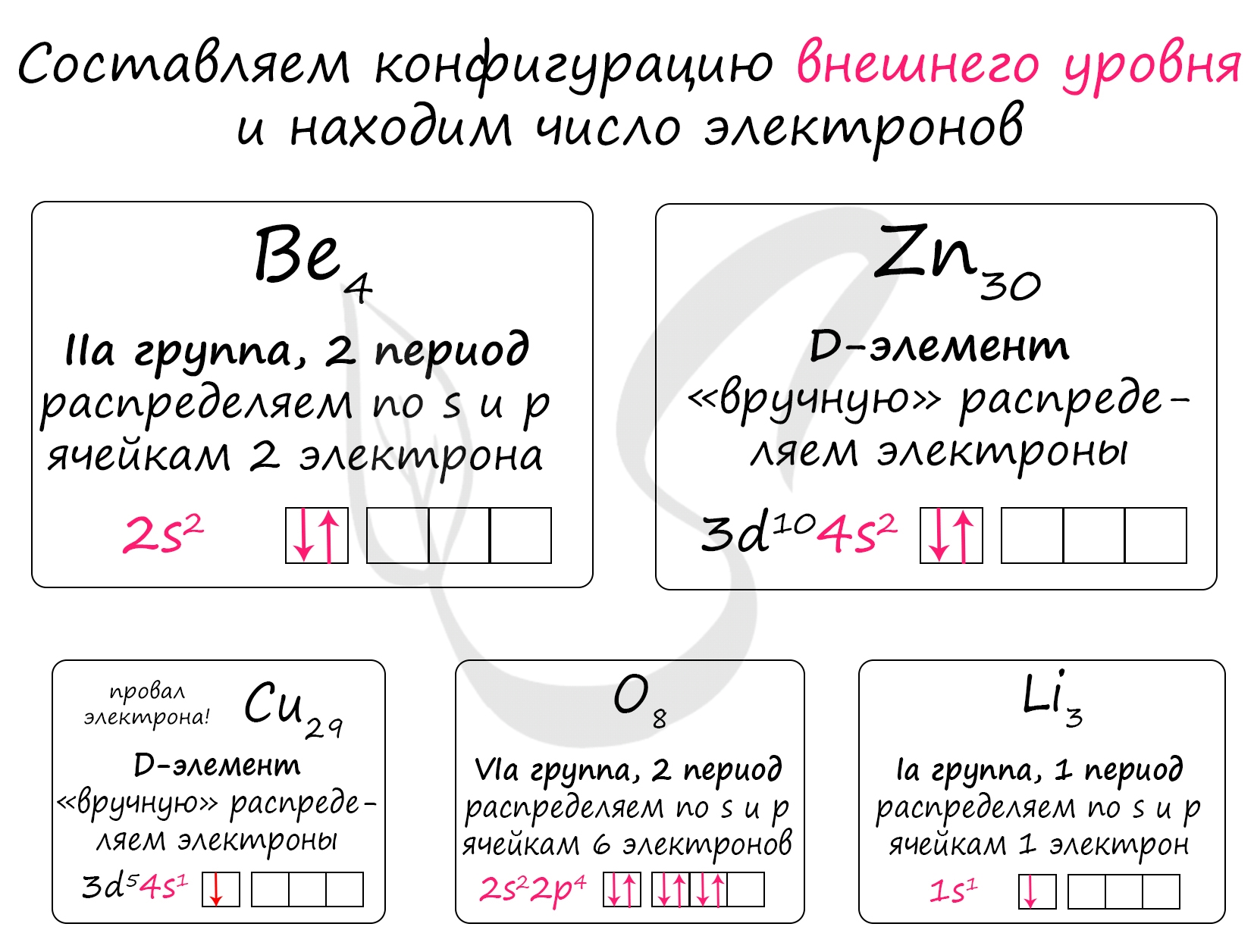
Выбранные элементы находятся в одном и том же периоде - 2. В периоде увеличение радиуса атома происходит справа налево (←), поскольку чем меньше электронов на внешнем уровне, тем радиус атома БОЛЬШЕ: электроны меньше притягиваются друг к другу и чувствуют себя более свободно :)
Радиус атома увеличивается: O → Be → Li
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6748.
Верный ответ: 14
Оксиды в степени окисления +1 образуют:
1) Li - постоянная степень окисления +1 (Li2O)
4) Cu - степени окисления +1 (Cu2O), +2 (CuO)
Остальные пункты:
2) Be - постоянная степень окисления +2 (BeO)
3) O - наиболее типичная степень окисления -2 (CaO), но также принимает -1 (пероксиды - Na2O2) и +2 (фторид кислорода - OF2)
5) Zn - постоянная степень окисления +2 (ZnO)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6749.
Верный ответ: 23
Ковалентные связи, образованные по донорно-акцепторному механизму, присутствуют в
2) HNO3 - в нитрат ионе [NO3]- есть ковалентная связь, образованная по донорно-акцепторному механизму
3) NH4Br - в ионе аммония [NH4]+ есть ковалентная связь, образованная по донорно-акцепторному механизму
Остальные пункты:
1) NaCl - ионная связь, образуется между атомами с большой разницей в электроотрицательности (чаще всего: типичный металл + типичный неметалл)
4) H2SO4 - ковалентные полярные связи (обменный механизм), между неметаллами H-O, O-S
5) H2O - ковалентные полярные связи (обменный механизм), между неметаллами H-O
Рекомендую выучить список веществ, образованных по донорно-акцепторному механизму:
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6750.

Верный ответ: 934
Под цифрами:
1 - гидроксид лития - щелочь (растворимое основание), проявляет основные свойства: реагирует с кислотами
2 - HCrO2 - хромистая кислота, просто записанная максимально хитро :)
3 - оксид лития - проявляет основные свойства, соответствует основанию LiOH
4 - кристаллогидрат сульфата меди, медный купорос
5 - гипофосфит калия, соль фосфорноватистой кислоты H3PO2 (H(PН2O2)) - сильная одноосновная кислота
6 - пероксид натрия (степень окисления натрия +1, а кислорода -1)
7 - тетрагидроксоцинкат(II) калия - комплексная соль
8 - оксид кремния (II) - несолеобразующий оксид
9 - дигидроортофосфат калия, кислая соль ортофосфорной кислоты (H3PO4), слабой трехосновной кислоты
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7101.
1) гидроксид калия
2) сульфат меди
3) серная кислота
4) метакремниевая кислота
5) гидросульфид натрия
Верный ответ: 25
В осадок выпадает сульфид меди(II) :
2CuSO4 + 2NaHS = 2CuS↓ + Na2SO4 + H2SO4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7418.
Верный ответ: 1354
В этом задании скрыты 60 реакций! Правильный подход к его выполнению может значительно повысить ваш уровень знаний неорганической химии.
Итак, ключевой момент: нужно попробовать составить реакцию каждого из веществ (А, Б, В, Г) со всеми предложенными реагентами! Вы должны узнать, возможна ли каждая из этих реакций, или понять причину, по которой она невозможна (например, в реакции не может быть два осадка: и справа, и слева). Следуйте такому подходу, и вы удивитесь, как быстро повысится ваш "неорганический уровень" ;)
Реакции для Fe2O3 протекают так:
Fe2O3 + K2CO3 = (t°) 2KFeO2 + CO2↑
Fe2O3 + 6HI = 2FeI2 + I2 + 3H2O
Fe2O3 + 3H2 = 2Fe + 3H2O
Реакции для NaOH протекают так:
4NaOH + P4 + 2H2O = 2PH3↑ + 2Na2HPO3
6NaOH + 3Cl2 = 5NaCl + NaClO3 + 3H2O
5NaOH + PCl3 = Na2HPO3 + 3NaCl + 2H2O
Реакции для SO2 протекают так:
SO2 + 2H2S = 3S + 2H2O
SO2 + H2O = H2SO3
SO2 + 2HNO3 = H2SO4 + 2NO2
Реакции для Cu протекают так:
Cu + 2H2SO4 = CuSO4 + 2H2O + SO2
2Cu + O2 = 2CuO
Cu + 2AgNO3 = Cu(NO3)2 + 2Ag
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6789.
Верный ответ: 6243
А) При термическом разложении нерастворимых оснований они легко отдают воду
Zn(OH)2 = (t°) ZnO + H2O
Б) В результате реакции обмена между гидроксидом цинка и азотной кислотой → образуется нитрат цинка и вода (не происходит изменения степеней окисления)
Zn(OH)2 + 2HNO3 = Zn(NO3)2 + 2H2O
В) Гидроксид цинка обладает амфотерными свойствами и в растворе с гидроксидом калия → образует комплексную соль
Zn(OH)2 + 2KOH = K2[Zn(OH)4] - тетрагидроксоцинкат калия
Г) В расплаве образование комплексной соли невозможно, так как при столь высоких температурах испаряется вода → образуется смесь оксидов калия и цинк - цинкат калия
Zn(OH)2 + 2KOH = (t°) K2ZnO2 + 2H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7595.
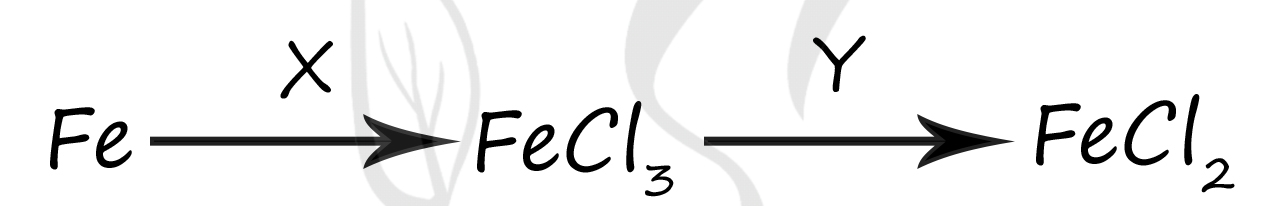
1) HNO3
2) NaCl
3) HCl
4) Fe
5) Cl2
Верный ответ: 54
Вещество X - (5) - Cl2
Хлор является сильным окислителем, окисляет железо именно до степени окисления +3 - наиболее устойчивой степени окисления железа (в отличие от хлора соляная кислота окисляет железо только до +2)
2Fe + 3Cl2 = 2FeCl3
Вещество Y - (4) - Fe
Эта реакция относится к реакциям по типу золотой середины: встречаются два атома железа +3 из хлорида железа (III) и железо в степени окисления 0 → промежуточная для них степень окисления будет +2, поэтому образуется хлорид железа (II)
Fe + 2FeCl3 = 3FeCl2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7911.
Верный ответ: 2431
А) Кетоны (бутанон) - общая формула R−(C=O)−R' - наличие карбонильной группы (С=O) у вторичного атома углерода
Б) Простой эфир (метилэтиловый эфир) - общая формула CnH2n+2O - наличие связи R-O-R'
В) Карбоновые кислоты (щавелевая - двухосновная карбоновая кислота) - общая формула HOOC-R-COOH наличие двух карбоксильных групп (две группы COOH)
Г) Первичный спирт (бутанол-1) - общая формула спиртов CnH2n+1OH - наличие гидроксильной группы, связанной с первичным атомом углерода

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6827.
Верный ответ: 24
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7038.
Верный ответ: 12345
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7599.
Верный ответ: 25
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7741.
Верный ответ: 3422
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7217.
Верный ответ: 4312
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7043.
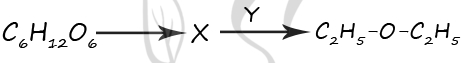
1) CH3COOH
2) H2SO4 (конц.)
3) C2H5OH
4) C2H5COOH
5) KOH (водн.)
Верный ответ: 32
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7534.
Верный ответ: 25
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7745.
Верный ответ: 12
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7186.
Верный ответ: 413
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7502.
Верный ответ: 2254
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6978.
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
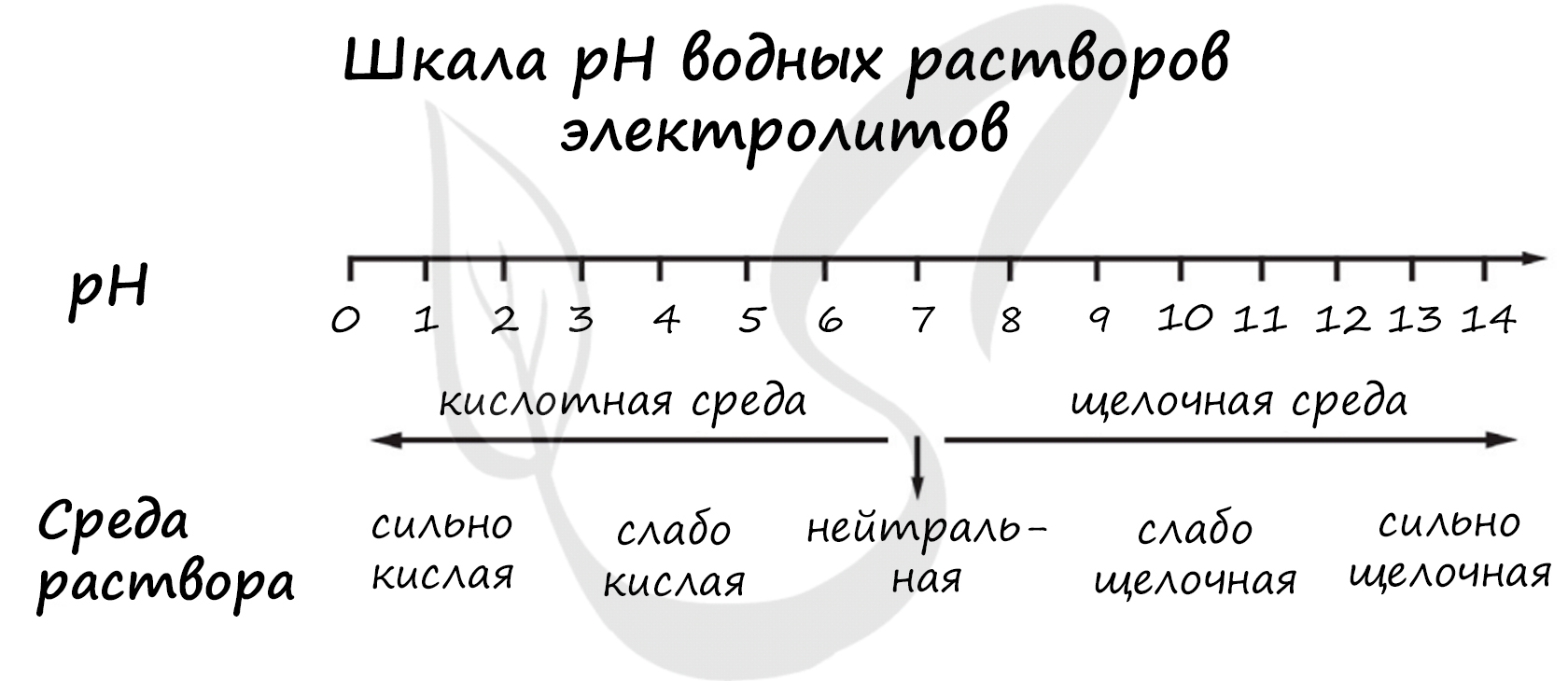
pH («пэ аш») - водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
1) бертолетова соль
2) фосфат цезия
3) сульфат марганца(II)
4) гидрофосфат цезия
Верный ответ: 2413
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6979.
Верный ответ: 3434
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7925.

Верный ответ: 62
Таблица (по условиям задания)
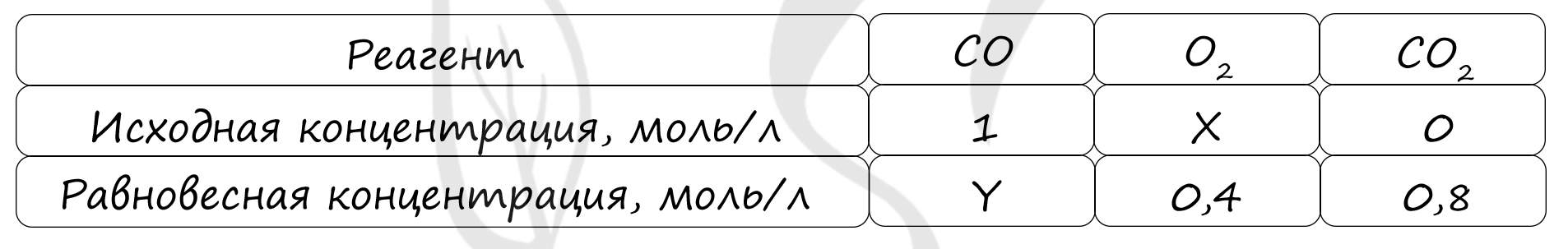
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7837.
Верный ответ: 3211
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7051.
Верный ответ: 421
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7927.
Ответом к заданиям 26-28 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Единицы измерения физических величин указывать не нужно.
Верный ответ: 1400
Найдем массу соли, которая присутствует в исходном растворе:
m(соли) = 600 · 0.1 = 60 грамм
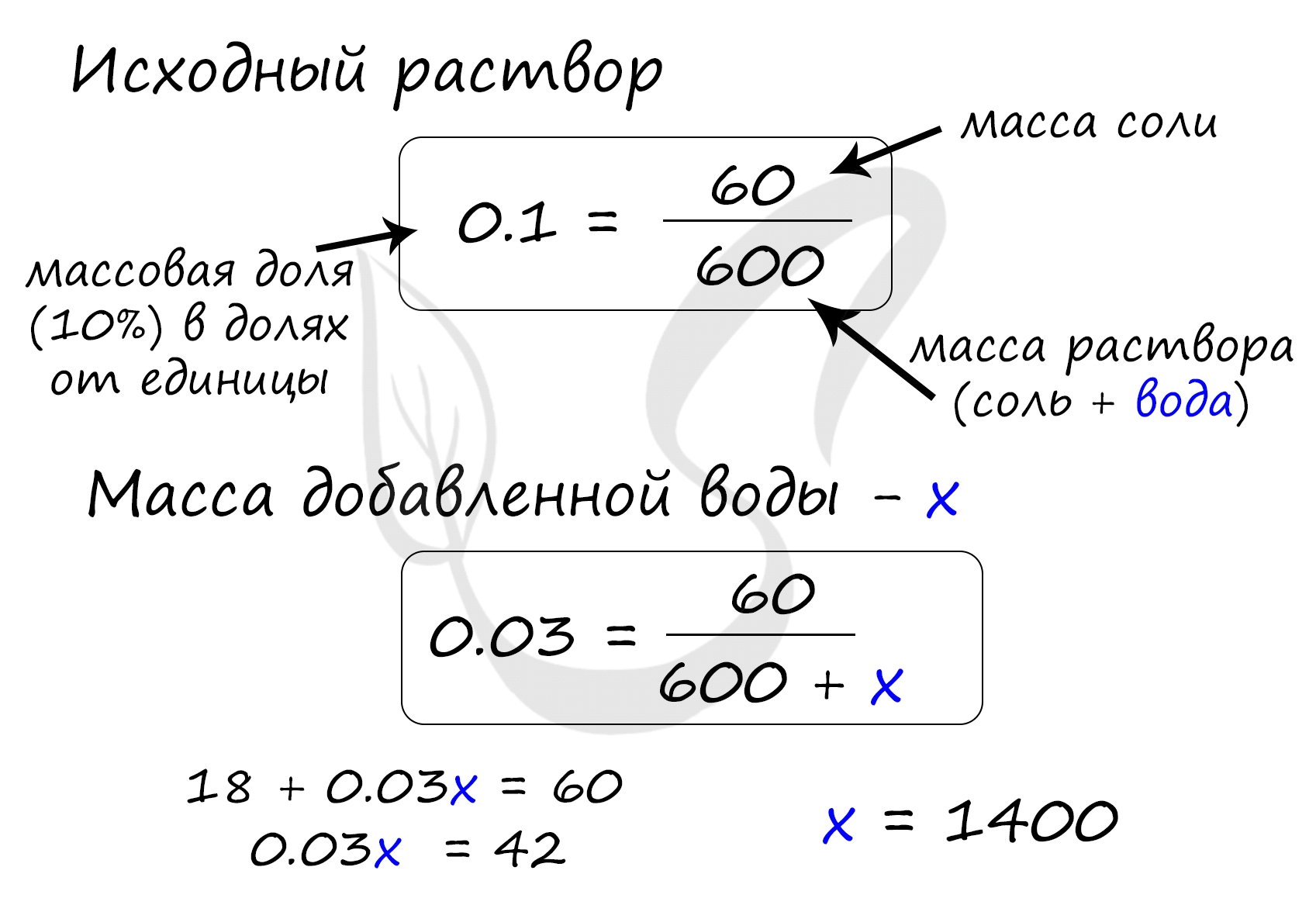
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7088.
Верный ответ: 18

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6844.
Верный ответ: 61,6
C + O2 = CO2
1) n(CO2) = v / Vr = 8,96 л / 22,4 л/моль = 0,4 моль
2) n(C) = n(CO2) = 0,4 моль
3) m(C) = n · Mr = 0,4 моль · 12 г/моль = 4,8 г
4) w(C) = 4,8 г / 12,5 г · 100% = 38,4%
5) w(примесей) = 100% - 38,4% = 61,6%
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7860.
Часть 2 Вы проверяете сами. Все пояснения и подсказки к частям 1 и 2 обязательно будут даны по окончании теста.
Для выполнения заданий 29,30 используйте следующий перечень веществ:
нитрит калия, хлорид алюминия, подкисленный раствор перманганата калия, гидроксид натрия, нитрат бария. Допустимо использование водных растворов веществ.
Возможна следующая реакция:
5KNO2 + 2KMnO4 + 3H2SO4 = K2SO4 + 5KNO3 + 2MnSO4 + 3H2O

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7231.

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7232.
1) CuO + CO = Cu + CO2↑
2) Cu + Cl2 = CuCl2
3) 2CuCl2 + 4KI = 2CuI + I2↓ + 4KCl
4) CuCl2 + 2AgNO3 = 2AgCl↓ + Cu(NO3)2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7408.
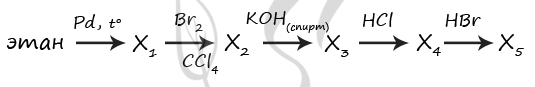
1) C2H6 = (t°, Ni) C2H4 + H2
2) C2H4 + Br2 = C2H4Br2
3) C2H4Br2 + 2KOH(спирт.) = C2H2 + 2KBr + 2H2O
4) C2H2 + HCl = CH2=CH-Cl
5) CH2=CH-Cl + HBr = CH3-CH(Br)Cl
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7374.
1) Вычислим количество вещества продуктов, массу и количество вещества кислорода
n(CO2) = 17,92 / 22,4 = 0,8 моль
n(C) = n(CO2) = 0,8 моль
n(H2O) = 18 / 18 = 1 моль
n(H) = 2n(H2O) = 2 моль
m(C + H) = 0,8 ⋅ 12 + 2 = 11,6 г
m(O) = 14,8 - 11,6 = 3,2 г
n(O) = 3,2 / 16 = 0,2 моль
Соотношение: C : H : O = 0,8 : 2 : 0,2 = 4 : 10 : 1
Простейшая формула C4H10O
2) Структурная формула CH3-CH2-CH2-CH2-OH
3) Уравнение реакции
CH3-CH2-CH2-CH2-OH + CuO = CH3-CH2-CH2-CHO + Cu +H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7306.
1) Уравнение реакции
СuSO4 + Fe = FeSO4 + Cu
2) Рассчитаем массу сульфата меди(II) в исходном растворе
n(СuSO4) = n(Сu) = n(Fe)
Чтобы найти эти количества вещества, рассчитаем массу СuSO4 в исходном растворе:
m(СuSO4)исх = 0,3 • 1,175 • 63,5 = 22,4 г.
3) После реакции количество вещества (по условию задачи), а следовательно, и масса CuSO4 уменьшились вдвое. Отсюда m(СuSO4)ост. = 11,2 г.
4) Вычислим количество вещества сульфата меди(II), израсходованного в реакции, изменение массы пластинки
n(СuSO4) = m/М = 11,2/160 = 0,07 моль.
Изменение массы пластинки составляет:
m(Сu) - m(Fe) = n•(M(Cu) - M(Fe)) = 0,07 • 8 = 0,56 г.
4) Вычислим массу пластинки после реакции: 7 + 0,56 = 7,56 г.
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7445.