


Верный ответ: 1542
А) Это банальная реакция обмена между гидроксидом хрома (III) и серной кислотой, важно сохранить исходную степень окисления хрома (+3), именно поэтому в продуктах мы выбираем сульфат хрома (III); вода образуется при соединении гидроксид-ионов основания и протонов кислоты
Cr(OH)3 + H2SO4 → Cr2(SO4)3 + H2O
Б) При реакции амфотерного гидроксида с основанием в растворе образуется комплексная соль
Cr(OH)3 + NaOH → Na3[Cr(OH)6]
В) При реакции амфотерного гидроксида с основанием при прокаливании (нагревании) образуются смешанные оксиды (хромит натрия это по сути смесь оксидов натрия и хрома), испаряется вода
Cr(OH)3 + NaOH → (t°) NaCrO2 + H2O
Г) При нагревании нерастворимые гидроксиды легко отдают воду, исходную степень окисления хрома (+3) сохраняем
Cr(OH)3 → (t°) Cr2O3 + H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7560.
Верный ответ: 1342
А) В результате реакции обмена между хлоридом алюминия и гидроксидом калия → образуется гидроксид алюминия (нерастворим, осадок) и хлорид калия
AlCl3 + 3 KOH = Al(OH)3↓ + 3KCl
Б) Угольная кислота, хоть и слабая, но сильнее кремниевой кислоты и способна вытеснять кремниевую кислоту из её солей - из силикатов: угольная кислота зашифрована в виде воды и углекислого газа;
В результате реакции обмена образуется нерастворимая кремниевая кислота, которая выпадает в осадок, и карбонат калия
K2SiO3 + 2HCl = 2KCl + H2SiO3↓
В) Соляная кислота безусловно сильнее кремниевой: вытесняет её (реакция обмена) из силиката калия → образуется нерастворимая кремниевая кислота и хлорид калия
K2SiO3 + 2HCl = 2KCl + H2SiO3↓
Г) Подобные реакции идут по типу двойного гидролиза: гидролиз хлорида алюминия приводит к образованию гидроксида алюминия, а гидролиз карбоната калия приводит к образованию угольной кислоты, которая неустойчивая и распадается на воду (вода входит в состав гидроксида алюминия) и углекислый газ
Те ионы, которые не подвергаются гидролизу: хлориды и калий - объединяются в хлорид калия
3K2CO3 + 2AlCl3 + 3H2O = 2Al(OH)3↓ + 3CO2↑ + 6KCl
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7525.
Верный ответ: 2614
А) При разложении гидрокарбонатов образуется карбонат, углекислый газ и вода
Ca(HCO3)2 = (t°) CaCO3 + H2O + CO2
Б) Получить гидрокарбонат можно реакцией средней соли (карбоната) с угольной кислотой - полная противоположность реакции в пункте А
CaCO3 + CO2 + H2O = Ca(HCO3)2
В) При реакции кислой соли с основанием → получают среднюю соль
Ca(HCO3)2 + Ca(OH)2 = 2CaCO3 + 2H2O
Г) В результате реакции обмена между гидрокарбонатом кальция и серной кислотой → образуется сульфат кальция и неустойчивая угольная кислота, которая сразу же распадается на воду и углекислый газ
Ca(HCO3)2 + H2SO4 = CaSO4 + 2H2O + 2CO2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7490.
Верный ответ: 5234
А) Здесь фактически в виде углекислого газа и воды зашифровали угольную кислоту: при реакции карбоната кальция с угольной кислотой → образуется кислая соль угольной кислоты - гидрокарбонат кальция
CaCO3 + CO2 + H2O = Ca(HCO3)2
Б) В реакции основного оксида с водой → получается основание (щёлочь), но только в случае если это основание растворимо: гидроксид кальция в рамках школьного курса и ЕГЭ - растворим(!), считается сильным основанием (щёлочью)
CaO + H2O = Ca(OH)2
В) Кальций активный металл: в ряду напряжения металлов стоит левее водорода, поэтому вытесняет водород из воды (воду можно представить в виде гидроксида HOH)
Ca + 2H2O = Ca(OH)2 + H2
Г) Почти лабораторный способ получения ацетилена (этина) - реакция карбида кальция с соляной кислотой (классический лабораторный способ - реакция карбида кальция с водой)
CaC2 + 2HCl = CaCl2 + C2H2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7455.
Верный ответ: 2221
А) Считать ли эту реакцию окислительно-восстановительный спорный вопрос: с одной стороны серная концентрированная кислота проявляет окислительные свойства и может окислить сульфит натрия до сульфата, но с другой стороны - здесь идёт обычная реакция обмена; в любом случае итоговая запись реакции сомнений не вызывает и записывается точно так же как пункт Б
Na2SO3 + H2SO4 = Na2SO4 + H2O + SO2
Б) Разбавленная серная кислота проявляет обычные кислотные свойства - не является окислителем, поэтому эта реакция будет идти по типу обмена, без изменения степеней окисления
Na2SO3 + H2SO4 = Na2SO4 + H2O + SO2
В) Концентрированная серная кислота проявляет окислительные свойства → под её действием сульфид натрия окисляется до сульфата натрия
Na2S + 4H2SO4 = Na2SO4 + 4H2O + 4SO2
Г) Разбавленная серная кислота проявляет обычные кислотные свойства - не является окислителем, поэтому эта реакция будет идти по типу обмена, без изменения степеней окисления
Na2S + H2SO4 = Na2SO4 + H2S
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7420.
Верный ответ: 6513
А) Реакция между хлоридом бария и разбавленной азотной кислотой не идёт, так как азотная кислота не может окислить такую соль: барий находится в максимальной степени окисления (+2) + по итогу
все (теоретически образующиеся) продукты растворимы (нет осадка, газа, слабого электролита)
BaCl2 + HNO3 → реакция не идет
Б) Реакция между карбонатом аммония и азотной кислотой идёт по типу обмена → образуется нитрат аммония и неустойчивая угольная кислота, которая сразу же распадается на воду и углекислый газ
(NH4)2CO3 + 2HNO3 = 2NH4NO3 + H2O + CO2
В) Реакция обмена между ацетатом натрия и азотной кислотой → приводит к образованию уксусной кислоты (более слабой, чем азотная; уксусная кислота является слабым электролитом) и нитрата натрия
CH3COONa + HNO3 = NaNO3 + CH3COOH
Г) В реакциях меди с разбавленной азотной кислотой выделяется оксид азота (II), а не оксид азота (IV), как в реакции меди с концентрированной азотной кислотой
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7385.
Верный ответ: 1221
А) В избытке гидроксида натрия в реакции с серной кислотой получается средняя соль, так как два атома натрия замещают два атома водорода кислоты
H2SO4 + 2NaOH = Na2SO4 + 2H2O
Б) В реакции гидроксида натрия с ортофосфорной кислотой при таком соотношении 2 атома натрия заменят 2 атома водорода кислоты, однако один атом водорода (третий атом водорода) кислоты останется, поэтому это будет кислая соль - гидрофосфат натрия
2NaOH + H3PO4 = Na2HPO4 + 2H2O
В) При соотношении 1 к 1 в реакции гидроксида натрия и серной кислоты → один атом натрия замещает один атом водорода кислоты, однако один атом водорода (второй атом водорода) кислоты останется, поэтому это будет кислая соль - гидросульфат натрия
H2SO4 + NaOH = NaHSO4 + H2O
Г) Реакция обмена с одноосновной кислотой приводит к образованию средней соли (кислых солей у соляной кислоты нет)
HCl + NaOH = NaCl + H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7350.
Верный ответ: 1353
Здесь нам очень пригодится схема термического разложения нитратов :)
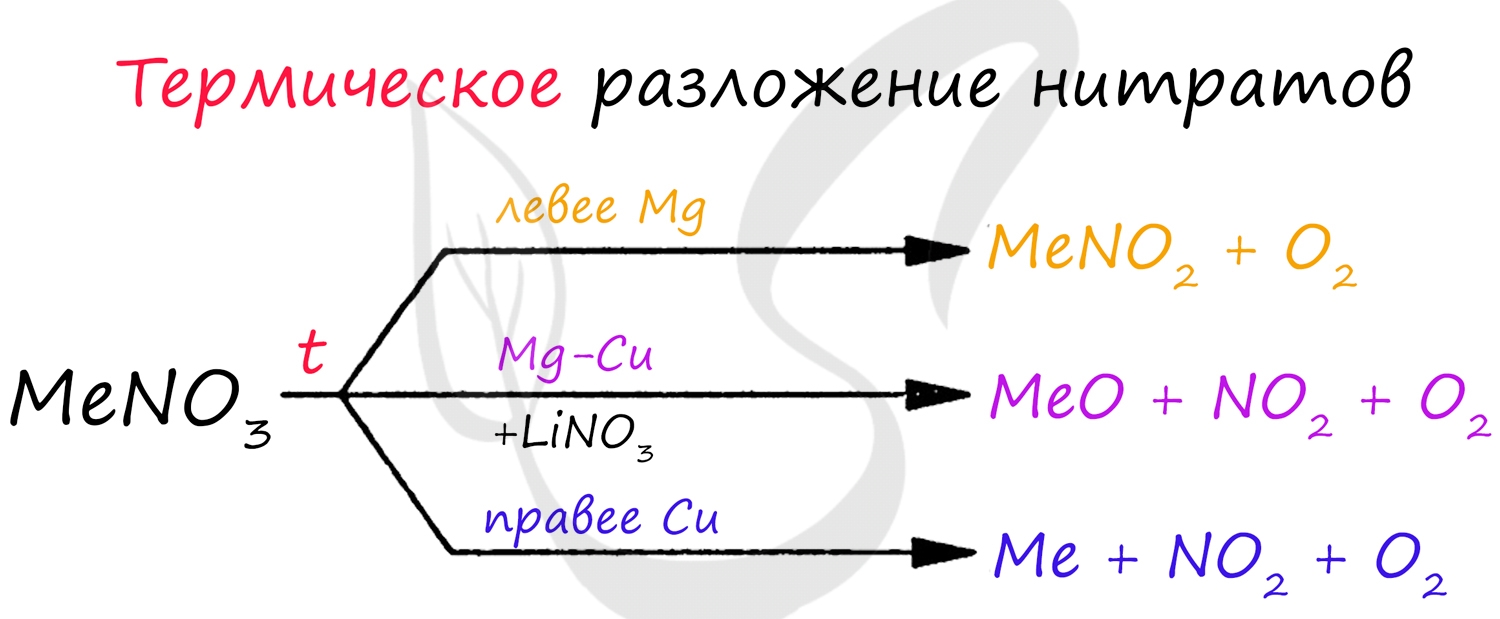
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7315.
Верный ответ: 4625
А) Концентрированная азотная кислота является сильным окислителем, в реакции с солью (сульфат железа (II)) будет происходить окисление железа +2 до железа +3, с выделением побочного газообразного продукта, который характерен для концентрированной азотной кислоты - это оксид азота (IV)
FeSO4 + 4HNO3(конц.) = NO2 + H2SO4 + Fe(NO3)3 + H2O
Б) Разбавленная серная кислота ведёт себя как самая обычная кислота (например соляная), и здесь будет вытеснение водорода цинком, так как цинк стоит в ряду напряжения металлов левее водорода (цинк более активен, чем водород)
Zn + H2SO4 = ZnSO4(разб.) + H2
В) Пероксид водорода является сильным окислителем, поэтому произойдёт окисление йодида (-1) до йода (0),
калий в присутствии сульфат-ионов образует сульфат калия
H2O2 + H2SO4 + 2KI = K2SO4 + 2H2O + I2
Г) В присутствии пары сильных окислителей железо +2 будет окислено до железа +3, а хром примет наиболее устойчивую для него его степень окисления +3 (куда хром - туда и калий, поэтому калий также образует сульфат)
6FeSO4 + K2Cr2O7 + 7H2SO4 = 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7280.
Верный ответ: 4432
А) В данном случае нам дали НЕ чистое вещество - НЕ медь, а гидроксид меди (II) - основные свойства, поэтому проводим обычную реакцию обмена без изменения степеней окисления → образуется нитрат меди (II) и вода
Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
Б) Аналогичная история как и в пункте А (см. пункт А) - нам дали не медь, а ОКСИД меди (II) - основные свойства
CuO + 2HNO3 = Cu(NO3)2 + H2O
В) В реакциях меди с концентрированной азотной кислотой выделяется оксид азота (IV), а не оксид азота (II) как в реакции меди с разбавленной азотной кислотой
Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
Г) В реакциях меди с разбавленной азотной кислотой выделяется оксид азота (II), а не оксид азота (IV) как в реакции меди с концентрированной азотной кислотой
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7245.