


1) ZnH2
2) Zn(OH)2
3) Zn
4) ZnO
5) ZnSO4
Верный ответ: 43
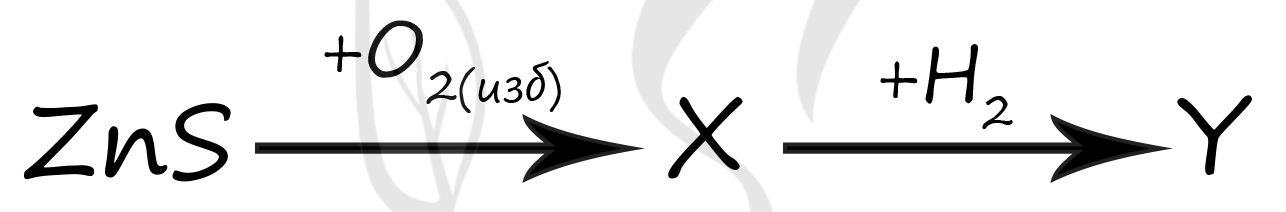
Вещество X - (4) - ZnO
При сгорании сульфида цинка → образуется оксид цинка (II) (это наивысший оксид цинка, у цинка постоянная степень окисления +2) и сернистый газ SO2 (для образования оксида серы (VI) - SO3 - нужен катализатор, о котором здесь ничего не сказано)
2ZnS + 3O2 = 2ZnO + 2SO2↑
Вещество Y - (3) - Zn
Водород является хорошим восстановителем: водород восстанавливает оксид цинка (II) до цинка в чистом виде
ZnO + H2 = Zn + H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7701.
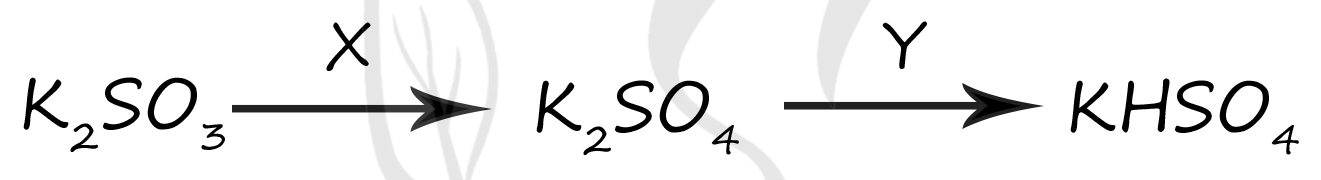
1) H2SO4
2) NaNO3(р-р)
3) SO2
4) NaOH
5) H2O2
Верный ответ: 51
Вещество X - (5) - H2O2
Чтобы получить из сульфита → сульфат, следует взять какой-нибудь окислитель - например пероксид водорода
K2SO3 + H2O2 = K2SO4 + H2O
Вещество Y - (1) - H2SO4
Чтобы получить из средней соли → кислую - следует добавить к средней соли соответствующую кислоту
K2SO4 + H2SO4 = 2KHSO4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7141.

1) Br2(р-р)
2) NaNO3(р-р)
3) SO2
4) NaOH
5) H2S
Верный ответ: 14
Вещество X - (1) - Br2(р-р)
Для окисления сернистой кислоты до серной нужен сильный окислитель, подойдёт бром (1)
H2SO3 + Br2 = H2SO4 + HBr
Cероводород (5) напротив является хорошим восстановителем, поэтому его выбирать не нужно
Вещество Y - (4) - NaOH
В реакциях оснований с многоосновными кислотами (в избытке) образуются кислые соли
NaOH + H2SO4 = NaHSO4 + H2O
Если бы в избытке было основание, то мы могли бы получить среднюю соль
2NaOH + H2SO4 = Na2SO4 + 2H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7106.

1) Br2(р-р)
2) HNO3(конц.)
3) SO2
4) NaOH
5) HCl
Верный ответ: 12
Вещество X - (1) - Br2(р-р)
Бром вытесняет серу, поскольку бром более активный неметалл, чем сера
Na2S + Br2 = 2NaBr + S
Вещество Y - (2) - HNO3(конц.)
Азотная кислота - сильный окислитель: сера будет окислена до серной кислоты, а побочным газообразным продуктом будет оксид азота (IV), поскольку азотная кислота была концентрированная
S + 6HNO3 = H2SO4 + 6NO2 + 2H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7036.
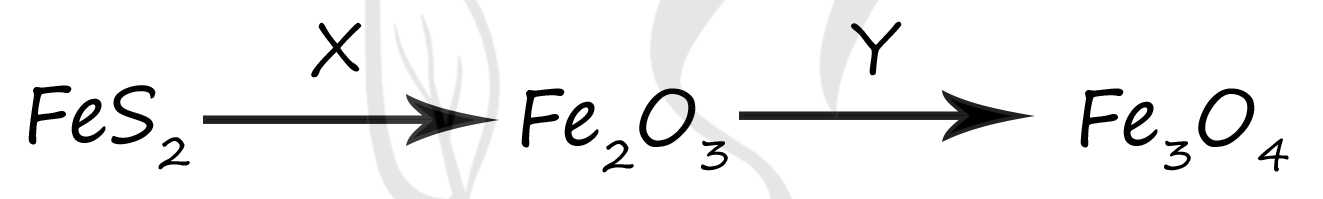
1) O2
2) HNO3(конц.)
3) Na2O
4) H2O
5) CO
Верный ответ: 15
Вещество X - (1) - O2
При сгорании дисульфида железа (пирита) образуется оксид железа (III) и сернистый газ
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
Вещество Y - (5) - CO
Железная окалина - Fe3O4 - это смесь двух оксидов (оксид железа (II) и оксид железа (III)), поэтому фактически наше задание сводится к получению оксида железа (II). Сделать это можно восстановив часть оксида железа (III) до оксида железа (II) хорошим восстановителем, например угарным газом
3Fe2O3 + CO = 2Fe3O4 + CO2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6826.