


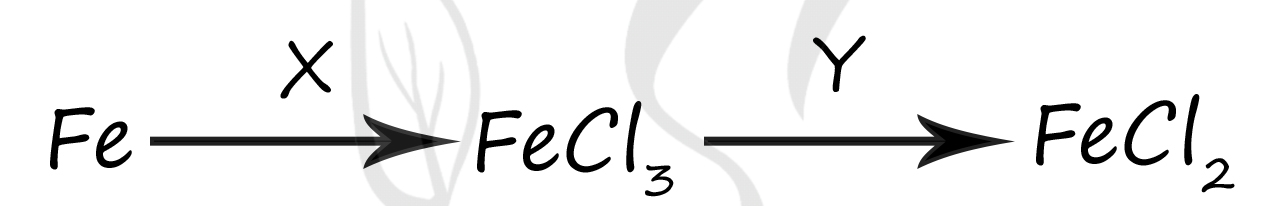
1) HNO3
2) NaCl
3) HCl
4) Fe
5) Cl2
Верный ответ: 54
Вещество X - (5) - Cl2
Хлор является сильным окислителем, окисляет железо именно до степени окисления +3 - наиболее устойчивой степени окисления железа (в отличие от хлора соляная кислота окисляет железо только до +2)
2Fe + 3Cl2 = 2FeCl3
Вещество Y - (4) - Fe
Эта реакция относится к реакциям по типу золотой середины: встречаются два атома железа +3 из хлорида железа (III) и железо в степени окисления 0 → промежуточная для них степень окисления будет +2, поэтому образуется хлорид железа (II)
Fe + 2FeCl3 = 3FeCl2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7911.

1) Ca(HCO3)2
2) CaH2
3) CaO
4) Ca(OH)2
5) Ca
Верный ответ: 34
Вещество X - (3) - CaO
При термическом разложение карбонатов → образуется оксид металла (в соответствующей степени окисления) и углекислый газ
CaCO3 = CaO + CO2↑
Вещество Y - (4) - Ca(OH)2
Основный оксид кальция реагирует с водой → с образованием основания, общая схема реакции: основный оксид + кислота = основание (щёлочь)
CaO + H2O = Ca(OH)2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7876.

1) ZnS
2) Zn3(PO4)2
3) CO2
4) ZnCl2
5) H2
Верный ответ: 54
Вещество X - (5) - H2
Водород является хорошим восстановителем, который восстанавливает цинк из оксида цинка (II)
ZnO + H2 = Zn + H2O
Вещество Y - (4) - ZnCl2
В реакции цинка с соляной кислотой цинк проявляет себя как более активный металл, стоящий в ряду напряжения левее водорода, и вытесняет водород из кислоты
Zn + 2HCl = ZnCl2 + H2↑
Однако почему не подходят сульфид цинка (1) или фосфат цинка (2)? Они являются нерастворимыми соединениями, а в самой последней реакции получается тоже нерастворимое соединение - гидроксид цинка (II). Нельзя из одного нерастворимого вещества (из одного осадка) получить другое нерастворимое вещество (другой осадок), поэтому в предпоследней реакции мы стараемся образовать именно какую-то растворимую соль цинка - идеально нам подходит хлорид цинка (II).
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7841.

1) гидроксид железа(III)
2) гидроксид железа(II)
3) сульфат железа(III)
4) сульфат железа(II)
5) железо
Верный ответ: 13
Вещество X - (1) - Fe(OH)3
В результате реакции обмена между хлоридом железа (III) и гидроксидом калия → образуется гидроксид железа (III) - ржавчина (осадок бурого цвета), и хлорид калия (нет изменения степеней окисления)
FeCl3 + 3KOH = Fe(OH)3↓ + 3KCl
Вещество Y - (3) - Fe2(SO4)3
В результате реакции обмена между гидроксидом железа (III) и сульфатом и серной кислотой образуется сульфат железа (III) и вода, общая схема реакции: основание + кислота = соль + вода (нет изменения степеней окисления)
2Fe(OH)3 + 3H2SO4 = Fe2(SO4)3 + 6H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7806.

1) гидрат аммиака
2) хлорид аммония
3) оксид азота(II)
4) аммиак
5) азотная кислота
Верный ответ: 42
Вещество X - (4) - NH3
Первая реакция представляет собой промышленный синтез аммиака
N2 + 3H2 ⇆ (t°, p) 2NH3
Вещество Y - (2) - NH4Cl
Аммиак проявляет основные свойства, охотно реагирует с кислотами → образуя соли аммония, общая схема реакции: основание + кислота = соль (в нашем случае образуется соль - хлорид аммония)
NH3 + HCl = NH4Cl
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7771.

1) сульфид железа(III)
2) гидроксид железа(III)
3) сульфит железа(II)
4) сульфат железа(II)
5) гидроксид железа(II)
Верный ответ: 54
Вещество X - (5) - Fe(OH)2
При реакции обмена между хлоридом железа (II) и гидроксидом калия (никто не меняет своей степени окисления!) → образуется гидроксид железа (II) и хлорид калия
FeCl2 + 2KOH = Fe(OH)2↓ + 2KCl
Вещество Y - (4) - FeSO4
При добавлении серной кислоты к нерастворимому гидроксиду железа (II) - кислота растворяет осадок → происходит реакция обмена, в ходе которой образуется сульфат железа (II) и вода (степени окисления никто не меняет, значит это была разбавленная серная кислота)
Fe(OH)2 + H2SO4 = FeSO4 + 2H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7736.
1) ZnH2
2) Zn(OH)2
3) Zn
4) ZnO
5) ZnSO4
Верный ответ: 43
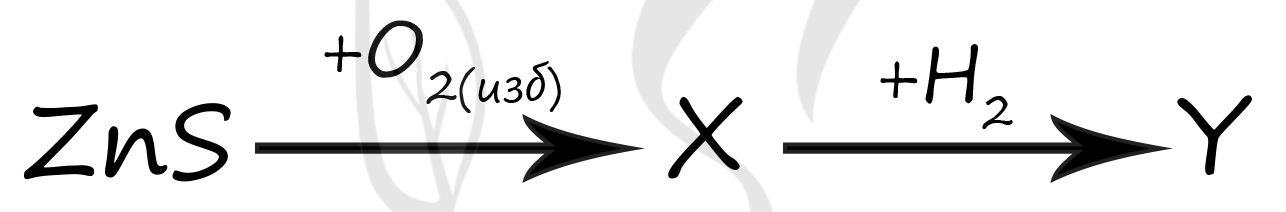
Вещество X - (4) - ZnO
При сгорании сульфида цинка → образуется оксид цинка (II) (это наивысший оксид цинка, у цинка постоянная степень окисления +2) и сернистый газ SO2 (для образования оксида серы (VI) - SO3 - нужен катализатор, о котором здесь ничего не сказано)
2ZnS + 3O2 = 2ZnO + 2SO2↑
Вещество Y - (3) - Zn
Водород является хорошим восстановителем: водород восстанавливает оксид цинка (II) до цинка в чистом виде
ZnO + H2 = Zn + H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7701.

1) H2O
2) NaOH
3) NaCl
4) HCl
5) Cl2
Верный ответ: 42
Вещество X - (4) - HCl
Амфотерный оксид цинка реагирует с соляной кислотой → с образованием соли и воды, степень окисления цинка постоянная +2 (не меняется)
ZnO + 2HCl = ZnCl2 + H2O
Вещество Y - (2) - NaOH
Реакция между хлоридом цинка и гидроксидом натрия идёт по типу обмена → в результате реакции образуется хлорид натрия и гидроксид цинка (II), который выпадает в осадок или в условиях избытка щёлочи (наш случай :) продолжает реакцию с гидроксидом натрия и образует растворимую комплексную соль
ZnCl2 + 4NaOH = Na2[Zn(OH)4] + 2NaCl
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7666.
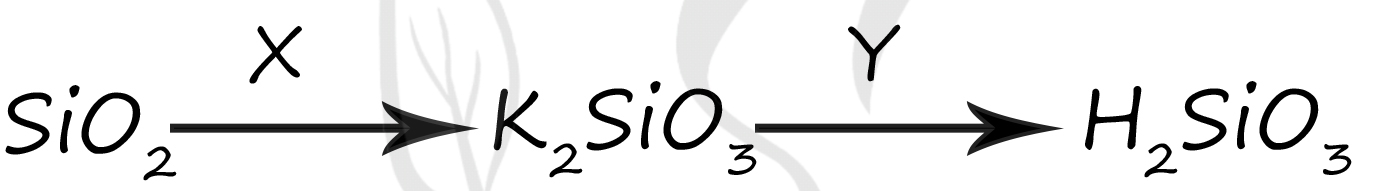
1) H2
2) HNO3
3) KCl
4) KOH
5) K2S
Верный ответ: 42
Вещество X - (4) - KOH
Оксид кремния (IV) является кислотным оксидом, в реакции с основанием приводит к образованию соли - силиката калия, общая схема реакции: кислотный оксид + основание = соль + вода (никто степени окисления не меняет)
SiO2 + 2KOH = K2SiO3 + H2O
Вещество Y - (2) - HNO3
В результате реакции обмена между силикатом калия и азотной кислотой → образуется нитрат калия и кремниевая кислота, которая выпадает в осадок
K2SiO3 + 2HNO3 = 2KNO3 + H2SiO3↓
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7631.

1) Al
2) AlCl3
3) Cl2
4) HCl
5) H2O2
Верный ответ: 14
Вещество X - (1) - Al
Перед нами пример алюминотермии: промышленного способа получения металлов, в ходе которого алюминий вытесняет другой металл из его соединения
8Al + 3Fe3O4 = 4Al2O3 + 9Fe
Вещество Y - (4) - HCl
Реакция железа с соляной кислотой приводит к окислению железа до +2 (важно помнить, что реакция с хлором окисляет железо до +3)
Fe + 2HCl = FeCl2 + H2↑
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7596.