

Общая формула вещества - CxHyOz
1) Вычислим количества веществ кислорода и водорода, их массу, сделаем проверку на кислород
n(CO2) = 7,04 : 44 = 0,16 моль
m(C) = 0,16 ⋅ 12 = 1,92 г
n(H2O) = 2,16 : 18 = 0,12 моль
n(H) = 2n(H2O) = 0,24 моль
m(H) = 0,24 ⋅ 1 = 0,24 г
M(CxHyOz) = 1,227 ⋅ 44 = 54 г/моль
nв-ва = 0,896 : 22,4 = 0,04 моль
mв-ва = n ⋅ M = 0,04 ⋅ 54 = 2,16 г
m(C) + m(H) = 1,92 + 0,24 = 2,16 г (кислород отсутствует)
Соотношение атомов: C : H = 0,16 : 0,24 = 1 : 1,5 = 2 : 3
Простейшая формула: C2H3
Молекулярная формула: C4H6
2) Структурная формула
CH3-CH2-C≡CH
3) Уравнение реакции
CH3-CH2-C≡C-H + [Ag(NH3)2]OH = CH3-CH2-C≡C-Ag↓ + 2NH3↑ + H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7061.
1) Уравнение реакций
2NaCl + 2H2O = 2NaOH + H2 + Cl2 (1)
2NaOH + 2AgNO3 = Ag2O↓ + 2NaNO3 + H2O (2)
NaCl + AgNO3 = AgCl↓ + NaNO3 (3)
2) Рассчитаем количество хлорида натрия и водорода
m(NaCl) = 227,5 ⋅ 0,18 = 40,95 г
n(NaCl) = 40,95 : 58,5 = 0,7 моль
n(H2) = 6,272 : 22,4 = 0,28 моль
3) Если бы хлорид натрия полностью подвергся электролизу, то количество выделившегося водорода составило бы 0,7 : 2 = 0,35 моль. По условию n(H2) = 0,28 моль, то есть прореагировал не весь хлорид натрия. Расчет по первому уравнению ведем по водороду.
4) Рассчитаем количество оставшегося NaCl
n(NaOH) = 2n(H2) = 0,56 моль
n(NaClразл.) = 2n(H2) = 0,56 моль
n(NaClост.) = 0,7 - 0,56 = 0,14 моль
5) Вычислим массовые доли веществ в осадке.
n(Ag2O) = 0,5n(NaOH) = 0,28 моль
m(Ag2O) = 0,28 ⋅ 232 = 64,96 г
n(AgCl) = n(NaClост.) = 0,14 моль
m(AgCl) = 0,14 ⋅ 143,5 = 20,09 г
ω(Ag2O) = 64,96 : (64,96 + 20,09) ⋅ 100% = 76,4%
ω(AgCl) = 20,09 : (64,96 + 20,09) ⋅ 100% = 23,6%
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7060.
Верный ответ: 25,3
Найдем массу соли, которая присутствует в исходном растворе:
m(соли) = 300 · 0.1 = 30 грамм

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7053.
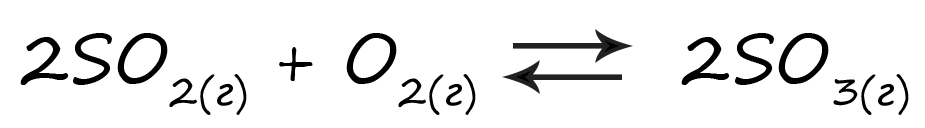
Верный ответ: 43
Таблица (по условию задачи)
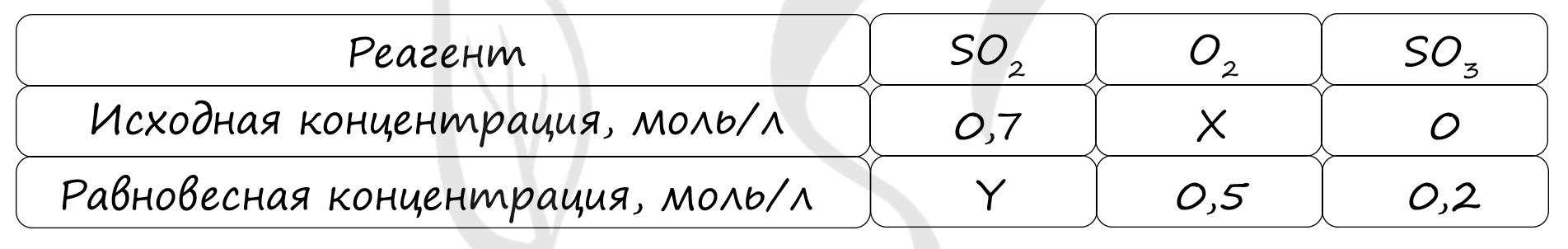
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7032.
1) Вещество - карбоновая кислота с общей формулой CnH2n+1COOH
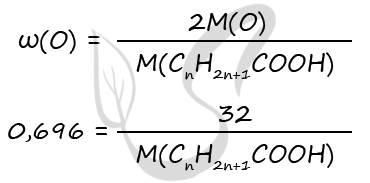

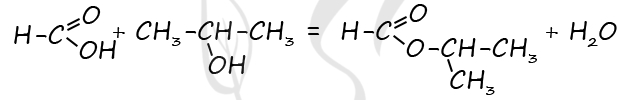
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 7026.