

1) Найдены количества вещества продуктов сгорания и определена молекулярная формула вещества:
n(CO2) = 2,69 : 22,4 = 0,12 моль
n(C) = 0,12 моль
n(H2O) = 2,16 : 18 = 0,12 моль
n(H) = 0,12 ⋅ 2 = 0,24 моль
n(N2) = 0,444 : 22,4 = 0,02 моль
n(N) = 0,02 ⋅ 2 = 0,04 моль
m(C + H + N) = 0,12 ⋅ 12 + 0,24 ⋅ 1 + 0,04 ⋅ 14 = 2,24 г
m(O) = 3,2 - 2,24 = 0,96 г
n(O) = 0,96 : 16 = 0,06 моль
n(C) : n(H) : n(N) : n(O) = 0,12 : 0,24 : 0,04 : 0,06 = 6 : 12 : 2 : 3
Молекулярная формула: C6H12N2O3
2) Структурная формула
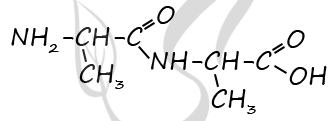
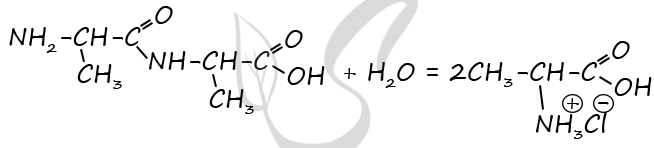
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6886.
1) Уравнения реакций:
2KCl + 2H2O = 2KOH + H2 + Cl2 (1)
2H2O = 2H2 + O2 (2)
4KOH + P2O5 = 2K2HPO4 + H2O (3)
2) Вычислим количества исходных веществ
m(KCl) = mр-ра · ω(KCl) = 80 · 0,25 = 20 г
n(KCl) = m : M = 20 : 74,5 = 0,268 моль
nобщ.(H2) = V : Vm = 8,96 : 22,4 = 0,4 моль
n(P2O5) = m : M = 9,514 : 142 = 0,067 моль
3) Вычислим количества соли калия и веществ, образовавшихся при электролизе
Если весь KCl вступит в реакцию (1), то выделится 0,134 моль водорода < 0,4 моль ⇒ начнется электролиз воды
n(KOH) = n(KCl) = 0,268 моль
n1(H2) = n1(Cl2) = 0,5n(KOH) = 0,134 моль
n2(H2) = nобщ.(H2) - n1(H2) = 0,4 - 0,134 = 0,266 моль
n(O2) = 0,5n2(H2) = 0,133 моль
n(KOH) : n(P2O5) = 0,268 : 0,067 = 4 : 1 ⇒ образуется гидрофосфат калия (коэфф.4 и 1)
n(K2HPO4) = 0,5n(KOH) = 0,134 моль
4) Вычислим массу выпавшего осадка
m(K2HPO4) = n · M = 0,134 · 174 = 23,316 г
mр-ра = mр-ра(KCl) - m(H2) - m(Cl2) - m(O2) + m(P2O5) = 80 - 2 · 0,4 - 71 · 0,134 - 0,133 · 32 + 9,514 = 74,94 г
m(H2O) = mр-ра - m(K2HPO4) = 74,94 - 23,316 = 51,624 г
В 100 г воды - 25 г соли
В 51,624 г воды - x г соли
x = 12,9 г = mраств.(K2HPO4)
m↓(K2HPO4) = m(K2HPO4) - mраств. = 23,316 - 12,9 = 10,416 г
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6885.
Верный ответ: 675
Найдем массу соли, которая присутствует в исходном растворе:
m(соли) = 450 · 0.1 = 45 грамм
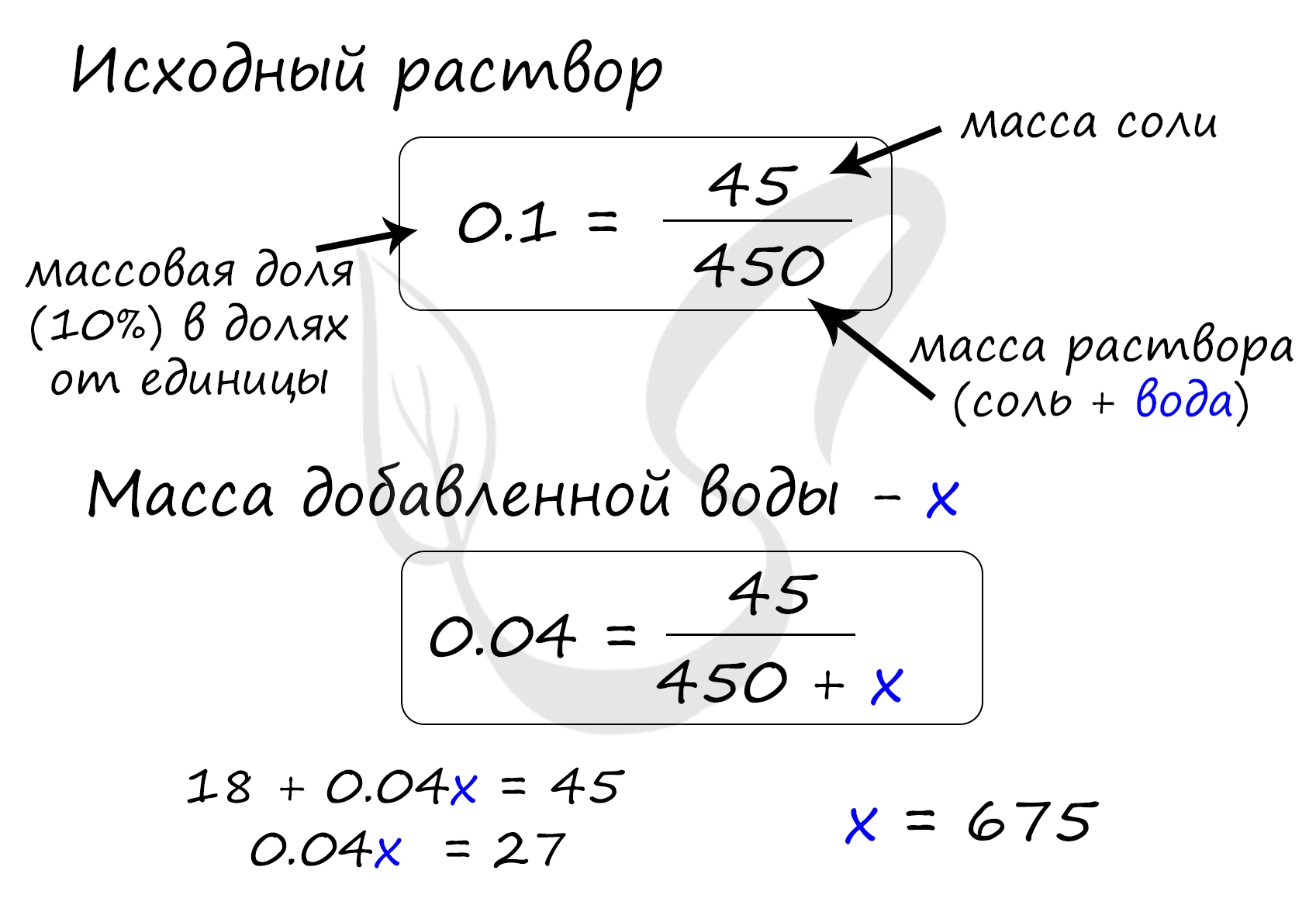
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6878.
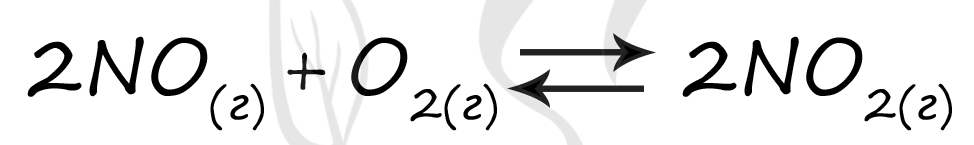
Верный ответ: 54
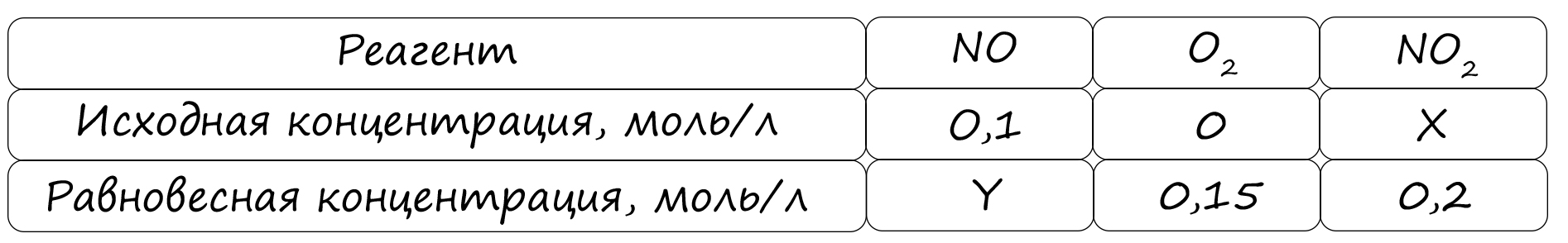
Таблица (по условиям задания)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6857.
1) Пусть формула вещества CxHyClz
Вычислим количества вещества углерода, водорода и хлора
n(CO2) = 9,9 : 44 = 0,225 моль
n(C) = n(CO2) = 0,225 моль
n(H2O) = 2,7 : 18 = 0,15 моль
n(HCl) = 3,36 : 22,4 = 0,15 моль
n(H) = 2n(H2O) + n(HCl) = 2 ⋅ 0,15 + 0,15 = 0,45 моль
n(Cl) = n(HCl) = 0,15 моль
Соотношение атомов составит:
x : y : z = 0,225 : 0,45 : 0,15 = 1,5 : 3 : 1 = 3 : 6 : 2
Молекулярная формула: C3H6Cl2
2) Структурная формула CH3-C(Cl2)-CH3
3) Уравнение реакции:
CH3-C≡CH + 2HCl = CH3-C(Cl2)-CH3
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6851.